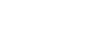Usan células madres para revertir la diabetes
Investigadores del Hospital Infantil de Boston, en Estados Unidos, han revertido con éxito la diabetes tipo 1 en un modelo de ratón mediante la inyección de células madre sanguíneas tratadas para producir más de una proteína llamada PD-L1, que es deficiente en ratones (y personas) con diabetes tipo 1. Las células reprimieron la reacción autoinmune en células de ratones y humanos e invirtieron la hiperglucemia en ratones diabéticos, como se detalla en un artículo publicado este miércoles en ‘Science Translational Medicine’.
“Realmente hay una remodelación del sistema inmunológico cuando se inyectan estas células”, afirma el investigador principal del estudio, Paolo Fiorina, del Hospital Infantil de Boston. El estudio muestra que las células madre tratadas, administradas a ratones, se instalan en el páncreas donde se forman las células de los islotes. Casi todos los ratones se curaron de la diabetes a corto plazo, y un tercio mantuvo los niveles normales de azúcar en la sangre durante toda su vida. El tratamiento fue efectivo si la producción de PD-L1 se estimuló mediante terapia génica o pretratamiento con moléculas pequeñas.
Estudios previos han intentado utilizar inmunoterapias para la diabetes tipo 1, con el objetivo de frenar el ataque autoinmune en las células de los islotes del cuerpo. Estos intentos han fracasado, en parte porque las terapias no se han dirigido específicamente a la diabetes. El trasplante autólogo de médula ósea, que infunde a los pacientes sus propias células madre sanguíneas para reiniciar su sistema inmunológico, ha ayudado a algunos pacientes, pero no a todos.
“Las células madre de la sangre tienen capacidades de regulación inmunitaria, pero parece que, en ratones y humanos con diabetes, estas capacidades se ven afectadas –destaca Fiorina, de la División de Nefrología del Hospital Infantil de Boston–. Encontramos que, en la diabetes, las células madre de la sangre son defectuosas, lo que promueve la inflamación y posiblemente el inicio de la enfermedad”.
Un equipo dirigido por Fiorina y el primer autor Moufida Ben Nasr, del mismo centro hospitalario, comenzó perfilando el transcriptoma de las células madresanguíneas para descubrir qué proteínas están produciendo las células. Utilizando un chip de ADN de expresión génica, encontraron que la red de factores reguladores genéticos (microARN) que controlan la producción de PD-L1 está alterada en células madre sanguíneas de ratones diabéticos y humanos; lo cual evita la producción de PD-L1, incluso temprano en la enfermedad.
Además, detectaron que PD-L1 tiene un potente efecto antiinflamatorio en el contexto de la diabetes tipo 1. PD-L1 se conoce como una “molécula de punto de control” inmune, que se une al receptor PD-1 (molécula de muerte programada 1) en las células T inflamatorias que se activan para causar reacciones autoinmunes, lo cual hace que las células T mueran o se vuelvan anérgicas (o inactivas).
Cuando Fiorina, Ben Nasr y sus colegas introdujeron un gen saludable para PD-L1 en las células madre, utilizando un virus inofensivo como portador, las células tratadas invirtieron la diabetes en los roedores. Fiorina y sus colegas también descubrieron que podían lograr el mismo efecto al tratar las células con un “cóctel” de tres moléculas pequeñas: interferón beta, interferón gamma y ácido polinésico-policitidílico.
“Creemos que la resolución de la deficiencia de PD-L1 puede proporcionar una nueva herramienta terapéutica para la enfermedad”, dice Ben Nasr. No obstante, Se necesitarán más estudios para determinar cuánto tiempo duran los efectos de la terapia celular y con qué frecuencia se debe administrar el tratamiento. “La belleza de este enfoque es la posible ausencia de efectos adversos, ya que utilizaría las propias células de los pacientes”, dice Fiorina.
En colaboración con científicos de ‘Fate Therapeutics’ (San Diego, California, Estados Unidos), Fiorina y sus colegas están trabajando para optimizar el “cóctel” de moléculas pequeñas utilizado para modular las células madre sanguíneas. El equipo mantuvo una reunión previa a la investigación de nuevos medicamentos (IND, por sus siglas en inglés) con la agencia estadounidense del medicamento para obtener su apoyo para realizar un ensayo clínico sobre la diabetes tipo 1.
Fuente: El Economista – España
Dispositivo reduce síntomas de abstinencia a opiáceos
Con la aprobación de su nueva indicación, el dispositivo de estimulación eléctrica NSS-2 Bridge de Innovative Health Solutions se puede utilizar en pacientes hasta por 5 días durante la fase de abstinencia física aguda, para aliviar los síntomas como sudoración, malestar gastrointestinal y agitación, insomnio y dolor en las articulaciones. El dispositivo es un pequeño estimulador eléctrico de nervios que se coloca detrás de la oreja del paciente y emite pulsos eléctricos para estimular las ramas de ciertos nervios craneales.
La aprobación se basa en datos de un estudio clínico de rama única revisada por la FDA. En el estudio, se evaluaron 73 pacientes sometidos a abstinencia física de opioides en función de su escala clínica de abstinencia de opiáceos (COWS). COWS es una evaluación clínica que mide los síntomas de abstinencia de opioides, como la frecuencia de pulso en reposo, sudoración, tamaño de la pupila, problemas gastrointestinales, dolor de huesos y articulaciones, temblores y ansiedad. Las puntuaciones oscilan entre 0 y más de 36, y las puntuaciones más altas representan síntomas más graves.
El puntaje promedio de COWS para los pacientes en el estudio antes de usar el dispositivo fue 20.1. Dentro de los 30 minutos de usar el dispositivo, los pacientes mostraron una reducción en los COWS de al menos 31%. El ochenta y ocho por ciento de los participantes en el ensayo cambiaron a terapia asistida con medicación después de 5 días de usar el dispositivo, junto con los medicamentos necesarios para síntomas persistentes, como náuseas y vómitos.
Este dispositivo ya fue aprobado por la FDA en 2014 para el uso en acupuntura.
Referencias
FDA grants marketing authorization of the first device for use in helping to reduce the symptoms of opioid withdrawal [news release]. FDA’s website. https://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm585271.htm?utm_campaign=11152017_PR_FDA%20allows%20marketing%20of%20opioid%20withdrawal%20device&utm_medium=email&utm_source=Eloqua.
Exitoso funcionamiento del páncreas artificial argentino
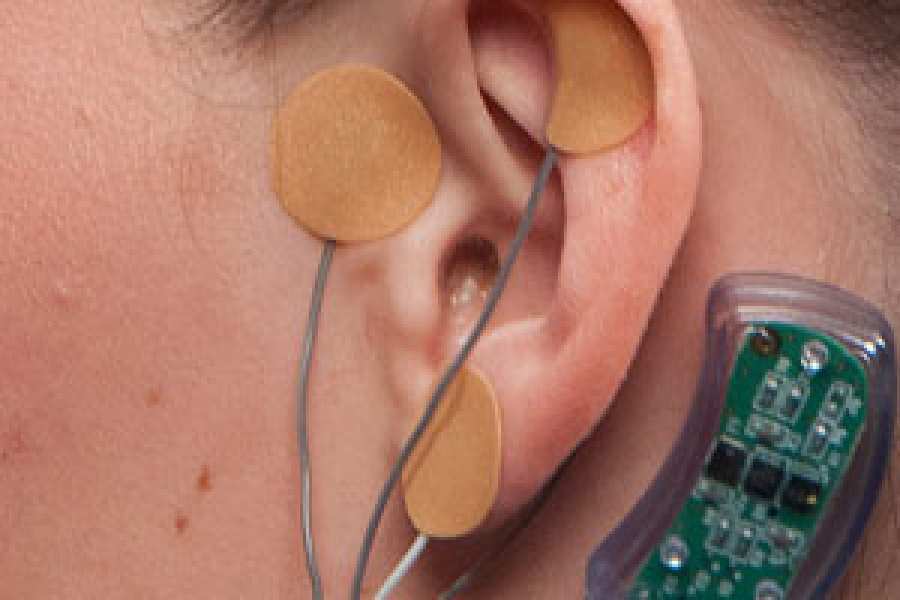
Un sistema de control automático que realiza las funciones del páncreas para regular los niveles de glucosa en sangre desarrollado en el país fue presentado este martes, con pruebas clínicas exitosas. Se trata del ARG – Automatic Regulation of Glucose -, un algoritmo que comanda la bomba de infusión de insulina en personas con diabetes tipo 1, obra de investigadores del Consejo Nacional de Investigaciones Científicas y Técnicas (CONICET) que trabajan en las sedes del Instituto Tecnológico de Buenos Aires (ITBA), Universidad Nacional de La Plata (UNLP) y Universidad Nacional de Quilmes (UNQ).
El sistema, que inyecta automáticamente la cantidad de insulina que la persona necesita en cada momento, está compuesto por un sensor continuo de glucosa, una bomba de infusión subcutánea de insulina y un Smartphone, en el cual se programa el algoritmo.
La primera fase de esta prueba clínica tuvo lugar en 2016 en el Hospital Italiano, que utilizó un algoritmo desarrollado en la Universidad de Virginia, Estados Unidos, que requería que el paciente calcule y registre en el sistema cuántos gramos de hidratos de carbono comerá para que la bomba infunda la insulina necesaria.
En junio de 2017, se realizó la segunda fase con el algoritmo ARG del ITBA-CONICET, el cual precisa únicamente que se registre el inicio de la comida, sin necesidad de calcular cuántos gramos de hidratos de carbono consumirá. En esta etapa participaron cinco pacientes adultos, hombres y mujeres, quienes pudieron mantener los niveles de glucosa dentro de un rango aceptable durante las 36 horas en que se probó el páncreas artificial.
El estudio, dirigido por el ingeniero Ricardo S. Sánchez Peña –investigador principal del CONICET que se desempeña como Director del Departamento de Investigación y Doctorado del ITBA-, contó con el apoyo del doctor Daniel Chernavvsky, médico argentino que trabaja en el Centro Tecnológico para la Diabetes de la Universidad de Virginia, así como también con el financiamiento de la Fundación Nuria en Argentina y Cellex en España, y la donación de las bombas de insulina del laboratorio Roche.
¿Cómo funciona el Páncreas Artificial?
El algoritmo fue diseñado para responder eficazmente a los aumentos de azúcar en sangre luego de las comidas y en las pruebas todos los pacientes lograron controlar este pico de glucemia mediante la acción del páncreas artificial.
El objetivo de este sistema es regular de forma automática el valor de azúcar en sangre, sin necesidad de que el paciente realice las correcciones con insulina habituales en el manejo de la diabetes tipo 1. Esto es importante porque las personas que utilizan bombas de infusión de insulina subcutánea invierten una gran cantidad de tiempo en calcular y programar la insulina necesaria para mantener sus niveles de glucosa sanguínea en rango. Muchas veces sufren hipoglucemias (azúcar baja en sangre) o hiperglucemia (azúcar elevada en sangre) como consecuencia de cálculos imprecisos, de la variabilidad que presenta cada individuo en cuanto a sus requerimientos, de imprevistos, entre otros.
Uno de los mayores temores de los pacientes que se infunden insulina es sufrir una hipoglucemia mientras duermen. Por ende, otro de los objetivos del páncreas artificial es lograr una mayor seguridad para el paciente mediante la disminución de hipoglucemias, especialmente las nocturnas. Durante la segunda fase del estudio, ninguno de los pacientes experimentó hipoglucemias graves como tampoco nocturnas.
Si bien los resultados son promisorios, es necesario continuar con estudios con la participación de un mayor número de personas. Es posible que en un futuro cercano esta nueva tecnología beneficie a muchos pacientes insulinodependientes.
Participaron del proyecto los investigadores del Conicet Ricardo S. Sánchez Peña, Demián García Violini y Marcela Moscoso Vázquez, todos con sede de trabajo en el ITBA; Patricio Colmegna, que se desempeña en la UNQ; Hernáb Battista, Fabricio Garelli, Emilia Fushimi y Nicolás Rosales por la UNLP; los doctores Luis Grosembacher, Cintia Rodríguez, Javier Giunta y Mariela Stasi del Hospital Italiano de Buenos Aires; los doctores Waldo H. Belloso, Ventura Simonovich, Valeria Beruto y Paula Scibona, del Servicio de Clínica Médica, sección Farmacología Clínica y el doctor Daniel Cherñavvsky, de la Universidad de Virginia, EE.UU.
Fuente: Ambito Financiero
Roche prueba en España el pago de tratamientos según su eficacia real
La multinacional farmacéutica Roche está probando en España un sistema por el que los servicios regionales de Salud pueden pagar el costo de los fármacos hospitalarios según la eficiencia real de los mismos en cada paciente al que se administre el tratamiento y no de manera global como hasta ahora. La plataforma tecnológica del laboratorio se puede usar además para todos los medicamentos del mercado y no solo para los que son propiedad del laboratorio suizo.
Actualmente, según señala Federico Plaza, director de Relaciones Institucionales de Roche España, seis comunidades autónomas en España ya han implantado este programa de manera experimental: Galicia, Navarra, Cataluña, Murcia, Baleares y Canarias. Y otras dos, Castilla y León y Madrid ya tienen previsto implantarlo. Además, en Andalucía y Cantabria se está estudiando su posible incorporación al sistema.
El programa se denomina MPR (Modelo personalizado de reembolso o Personalized Reimbursement Models (PRM) en inglés) y es un nuevo modelo de financiación de fármacos innovadores, pensado para que el precio a pagar por la administración derive de los beneficios directos que genera para el paciente. España es uno de los países pioneros donde Roche ha empezado a implementar este modelo.
La primera novedad que introduce el modelo de Roche es que se puede medir el uso de cada fármaco según para la indicación en la que trate al paciente. De esta manera, según explican los responsables de la filial española, cada una de estas indicaciones puede tener un precio distinto, acorde al valor que el fármaco está aportando en el caso concreto.
Precio por cada indicación
Hasta ahora, aseguran desde Roche, cuando un fármaco llega al mercado lo hace con un precio fijado por la administración para una primera indicación, es decir una patología concreta. Si el fármaco posteriormente muestra que también es eficaz en otra indicación -otro grupo de pacientes- lo que hace la administración es bajar el precio que paga por él, porque se estima que se usará en más pacientes y el laboratorio tendrá más ventas. “La idea es que cada indicación tenga un precio en función de su utilidad terapéutica. En los casos en los que sea más disruptiva, el precio será más elevado; pero habrá otras indicaciones donde se compruebe que el uso es menor o con menores resultados y se pueda pagar menos”, indica Federico Plaza.
Además, este modelo podría suponer un incentivo para las compañías para que se centren en innovaciones relevantes y no como hasta ahora, que se penalizan las nuevas indicaciones. El sistema será realmente útil con la llegada de la inmunoterapia en el tratamiento del cáncer, cuyos fármacos serán eficaces hasta para 30 indicaciones distintas.
Fuente: El Economista – España
El Senado español propone más peso para servicios farmacéuticos
La Comisión de Sanidad y Servicios Sociales del Senado español creará, a iniciativa del Grupo Popular, una ponencia de estudio sobre el desarrollo de servicios profesionales farmacéuticos asistenciales desde el Sistema Nacional de Salud (SNS).
La ponencia ha sido impulsada a través de una moción que se ha debatido este martes en el seno de dicha Comisión y cuenta con el apoyo de todos los grupos de la oposición en la Cámara Alta, por la “enorme importancia” que puede jugar el farmacéutico de cara al progresivo envejecimiento de la población y el aumento de las enfermedades crónicas.
“El farmacéutico, por su preparación y competencias profesionales, y la farmacia comunitaria, por su cercanía y accesibilidad a los pacientes, representan dos pilares fundamentales sobre los que construir cualquier estrategia de cronicidad”, destacan los ‘populares’ en su propuesta.
Estos servicios profesionales engloban aquellas actividades prestadas desde la farmacia relacionadas con la prevención de enfermedad y la mejora de la salud de la población, mediante un papel activo del farmacéutico en la optimización del proceso de uso y los resultados de los tratamientos.
Entre otros, según ha detallado el senador ‘popular’ Francisco José Fernández en la defensa de la iniciativa, estarían el control de la adherencia terapéutica, la revisión de botiquines, el seguimiento farmacoterapéutico, la realización de medidas antropométricas, determinación de parámetros clínicos, educación sanitaria o asesoramiento nutricional.
Y para alinearse con los objetivos generales del sistema sanitario, deben tener entidad propia y contar con unos procedimientos y sistemas de documentación que permitan su evaluación y retribución, para “garantizar su universalidad, continuidad y universalidad”.
Información de medicamentos prescritos
En la ponencia se estudiará el impulso de estos servicios profesionales y el acceso a la información relativa a los medicamentos que el paciente está utilizando, “tanto prescritos en el sistema público como privado, con o sin receta, especialmente en pacientes crónicos y polimedicados”.
Sobre todo, según ha recordado, porque estos servicios permiten “contemplar ahorros” para el SNS y contribuir a su sostenibilidad, ya que ayuda a reducir los problemas de salud no controlados y las urgencias. De hecho, Fernández ha reconocido que también podría contemplar la remuneración de estos servicios mediante acuerdos entre colegios profesionales y las comunidades autónomas.
Durante el debate de la moción el PP rechazó una enmienda del Grupo Unidos Podemos-En Comú Podem-En Marea para que en la ponencia también se analizara el impacto que ha tenido el nuevo sistema de copago farmacéutico, que introdujo el Gobierno mediante la reforma sanitaria de 2012, en la falta de adherencia al tratamiento.
Para ver la ponencia que se hizo en el Senado: http://bit.ly/2zDXc5w
Fuente: Redacción Médica – España
Anmat prohíbe suplemento dietario
La Administración Nacional de Medicamentos y Tecnología Médica (ANMAT) prohibió la comercialización del suplemento dietario “Forskolin 250″ Food Suplement 60 tabletas, elaborado en el Reino Unido.
Así lo indica la Resolución 11571-E/2017, que fue publicada en el Boletín Oficial de este miércoles.
“El producto se halla en infracción al artículo 4° de la Ley 18284, al artículo 4° del Anexo II del Decreto 2126/71 y a los artículos 13 y 155 del Código Alimentario Argentino (CAA), por carecer de autorización de producto y de establecimiento, resultando ser un producto ilegal”, argumentó la autoridad regulatoria.
Y agrega: “Por tratarse de productos que no pueden ser identificados en forma fehaciente y clara como producidos, elaborados y/o fraccionados en un establecimiento determinado, no podrán ser elaborados en ninguna parte del país, ni comercializados ni expendidos en el territorio de la República de acuerdo a lo normado por el artículo 9° de la Ley 18284″.
Fuente: Diario Veloz
Día Mundial de la Diabetes: por qué falla el tratamiento?
El Día Mundial de la Diabetes, instituido por iniciativa de la Federación Internacional de la Diabetes y la OMS, se celebra el 14 de noviembre para conmemorar el aniversario del nacimiento de Frederick Banting, quien, junto con Charles Best, tuvo un papel determinante en el descubrimiento en 1922 de la insulina, hormona que permite tratar a los diabéticos y hacer su vida saludable.
Un factor común que sucede en todas partes del mundo es alto índice de pacientes con diabetes que no logra cumplir con los objetivos que propone el profesional que los atiende. Esto se debe a varios factores pero fundamentalmente a dos.
Por un lado, desde el punto de vista del tratamiento médico, por lo general es muy poco el tiempo que se dispone para una consulta médica y esto dificulta una mirada integral del tratamiento y de los resultados obtenidos. Más tiempo dedicado al paciente es mayor conocimiento del paciente lo que permitiría ajustar y personalizar el tratamiento hacia la necesidad y requerimiento de cada persona en cada momento.
Por otro lado, existe un factor sociocultural, debido a que existen muchas presiones externas al paciente, del contexto social, que aumentan la resistencia al cambio de hábitos de las personas con diabetes hacia una vida más sana, menos sedentaria y con una alimentación balanceada. Constantemente hay una invasión de alimentos y costumbres que fomentan un alto consumo de productos azucarados y una pulsión hacia el estilo de vida sedentaria.
Se estima que del 70 al 80% de las personas con diabetes bajo tratamiento no logra alcanzar los objetivos planteados por el profesional. En los últimos Congresos mundiales se ha instalado el concepto de realizar una atención médica mediante un método integral para los pacientes con diabetes que incluya una mirada nutricional, psicológica, sociológica y deportiva. La integración de las diversas ramas médicas, aporta y detecta de qué manera el paciente se desenvuelve a diario, realiza tareas, cómo se comporta con su organismo para poder reducir el impacto negativo del medio ambiente sobre la enfermedad.
Del mismo modo, ese nuevo tratamiento integral debe realizar un balance equilibrado que permita optimizar el tratamiento farmacológico e incorporar los adelantos tecnológicos que ya están disponibles e ir preparando el terreno para los próximos que ya vendrán.
Según la OMS, actualmente hay en el mundo 422 millones de personas con diabetes. En Argentina, la diabetes afecta a 1 de cada 10 personas mayores a 18 años. Para mejorar la calidad de vida de los pacientes con diabetes y evitar que estas cifras sigan una tendencia creciente es de suma relevancia que el tratamiento este acompañado por un cuerpo médico integrado y que a su vez, el paciente lleve adelante hábitos saludables.
-
Actualmente hay 442 millones de personas que padecen diabetes
-
Es la causa del 5% del total de las muertes del mundo.
-
Más del 80% de las muertes por diabetes se registran en países de ingresos bajos y medios
-
La mitad de las muertes corresponden a personas de menos de 70 años y un 55% a mujeres.
-
80% de los pacientes tiene diabetes tipo 2. Se monitorea menos en lo global.
-
La diabetes no se cura, se mejora el medio ambiente hostil donde se desarrolla.
-
En Argentina la Diabetes afecta a 1 de cada 10 argentinos mayores de 18 años
-
45% de subdiagnóstico. Personas que portan la enfermedad y no lo saben.
-
Un paciente con diabetes tipo 1 recibe 10 mini agresiones hacia el cuerpo por día (monitoreo + pinchazo)
Las universidades incorporarán a 340 investigadores del Conicet
El año pasado, esos docentes investigadores con formación doctoral habían quedado seleccionados pero no habían sido incorporados a la carrera de investigador del organismo.
La cantidad de investigadores seleccionados pero no incorporados a las carreras del Conicet asciende a 390. De ese total, 340 serán incorporados a 42 universidades públicas nacionales como docentes investigadores con dedicación exclusiva, mientras que los 50 restantes “aún no acordaron su ingreso a ninguna universidad”, informó el ministerio de Educación.
El año pasado, esos docentes investigadores con formación doctoral habían sido seleccionados y, su selección, aprobada y recomendada por el Conicet, pero no habían sido incorporados a la carrera de investigador del organismo.
El Ministerio precisó que a través de la Secretaría de Políticas Universitarias “aportará el financiamiento para la creación de cargos o el incremento de las dedicaciones necesarias para la incorporación a las universidades de esos doctores”.
El 33 % de los investigadores fueron incorporados a universidades de la región metropolitana, el 28% a la bonaerense, el 18% a la región centro del país, el 8% a Nuevo Cuyo, el 6% al NOA, el 4% al sur y el 3% al NEA.
En tanto, de los 340 investigadores que se incorporarán a las universidades, el 25% corresponden al área de las Ciencias Naturales y Exactas, el 23 a las Ciencias Sociales, el 20 a las Agrícolas y Ambientales, el 17 a las Humanas, el 11 a las Ingenierías y Tecnologías y el 5 a las Ciencias Médicas y de la Salud.
El conflicto se inició a fines del año pasado cuando el Conicet decidió que la mitad de los investigadores que habían sido aprobados para ingresar a la carrera de doctorado dentro de ese organismo no lo iban a hacer por una cuestión presupuestaria.
En medio de las disputas a lo largo de este año, el Ministerio de Ciencia y Técnica y el de Educación acordaron que ingresen a las universidades, aunque los gremios pedían que se mantenga la estabilidad laboral y la equivalencia salarial con el Conicet.
Los becarios mantenían la inquietud a raíz que esas becas vencían en diciembre y aún no habían formado los contratos con las universidades y corría riesgo de no percibir becas ni contratos entre enero y abril.
Fuente: Agencia Télam
Nuevo mecanismo frena avance de tumores pediátricos
|
|
||
|
|
||
| El Centro de Investigación Biomédica en Red de Cáncer (CIBERONC), a través del grupo de investigación liderado por Xosé R. Bustelo, perteneciente también al Centro de Investigación del Cáncer de Salamanca, acaba de descubrir que el gen VAV1, habitualmente implicado en la formación de una amplia gama de tumores, puede también ejercer papeles implicados en la supresión de algunos tipos específicos de leucemia linfoblástica aguda de linfocitos T. Esta leucemia es el cáncer pediátrico más frecuente y, todavía hoy, tiene muchos retos para un diagnóstico y tratamiento adecuados. Este descubrimiento acaba de ser publicado en Cancer Cell.
Los linfocitos T son células del sistema inmune que tienen por función el reconocimiento y destrucción de células de nuestros órganos que se han convertido en cancerosas o que han sido infectadas por virus u otros patógenos. También están a cargo de la regulación de otras células del sistema inmune implicadas en la destrucción de cualquier agente externo que invada nuestro organismo como pueden ser productos químicos o bacterias. Pese a estas funciones positivas, los linfocitos T sufren en algunos casos alteraciones genéticas que los hacen pasar de agentes protectores a células malignas causantes de tumores. Uno de los cánceres más frecuentes que se originan a partir de estas células es la denominada leucemia linfoblástica aguda de linfocitos T (LLA-T). Este tumor es el más frecuente en niños en nuestro país y también afecta a un número significativo de adultos. Los porcentajes de curación de esta enfermedad han mejorado a lo largo de estos últimos años, aunque todavía presenta importantes retos como son el tratamiento de pacientes que son resistentes a las terapias actuales o que recaen tras la aplicación de las mismas. Debido a ello, la supervivencia de los pacientes con estos tumores (68% de los casos) es todavía hoy muy mejorable desde el punto de vista clínico. La formación de LLA-T, al igual que en muchos otros cánceres, está causada por la acumulación de múltiples alteraciones genéticas. Estas alteraciones, denominadas mutaciones, causan la activación de genes que actúan como “aceleradores” de la malignización de las células y, al mismo tiempo, la inactivación de otros genes que actúan como “frenos” del proceso de tumorigénico. Éstos últimos genes frenan el crecimiento de las células que han sufrido alteraciones genéticas o, alternativamente, inducen la muerte de las mismas a través de un mecanismo conocido como “suicidio celular”. El objetivo de la medicina personalizada es que, a través del conocimiento de estas alteraciones genéticas, se puedan desarrollar terapias adecuadas que permitan la eliminación de las células cancerosas. Sin embargo, un gran problema que existe en este campo es que, dados los múltiples cambios genéticos que una célula tumoral alberga, es difícil identificar los genes alterados que actúan como acelerador y freno en la formación de tumores. Una complicación adicional es que muchas de estas alteraciones son diferentes dependiendo del tipo tumoral que se estudie y, en muchos casos, incluso del subtipo clínico de un mismo tumor. En un artículo que se publica hoy en la revista Cancer Cell, una investigación multicéntrica liderada por el CIBERONC y el Centro de Investigación del Cáncer de Salamanca ha identificado un gen que actúa como un freno clave en la formación de la LLA-T. A través del uso de ratones modificados genéticamente, líneas celulares representativas de LLA-T y células derivadas de pacientes, este trabajo permitió identificar a VAV1 como uno de genes supresores que evitan la formación de estos tumores y, posteriormente, establecer el mecanismo molecular que media este efecto antitumoral. Este mecanismo se basa en controlar los niveles de una proteína, denominada ICN1, que actúa como acelerador en la formación de estos tumores. Como resalta el Dr. Bustelo, “Nuestro trabajo ha demostrado que VAV1, a través de la formación de un complejo multiproteico con la proteína CBL-B, “come” literalmente al acelerador ICN1 haciendo que éste desaparezca de las células tumorales. Esto hace que se pare el crecimiento de las mismas y que eventualmente se mueran”. El trabajo también ha identificado la estrategia que las células tumorales desarrollan para eliminar este freno, el cual se basa la generación de alteraciones genéticas que provocan la activación espuria de unas proteínas denominadas TLX. Éstas reprimen la expresión del gen VAV1 en las células tumorales mutadas y, como consecuencia, “borran” el freno que para la expansión incontrolada de las mismas. “Pese a ello – añade el Dr. Bustelo– hemos podido demostrar que si reactivamos VAV1 podemos volver a parar el crecimiento de estas células alteradas genéticamente e inducir su muerte de forma muy rápida. Esto sugiere que, a largo plazo, podría ser factible el diseño de vías terapéuticas que pudiesen reproducir el mismo efecto en pacientes”. VAV1 muestra un comportamiento de Dr. Jekyll o Mr. Hyde dependiendo del tipo tumoral Una sorpresa que surgió en este trabajo fue el hecho mismo del descubrimiento de VAV1 como un gen implicado en la supresión tumoral. Ello se debe a que trabajos previos habían demostrado que este gen y otros similares favorecen el crecimiento y metástasis de diversos tipos tumorales. Según destaca el primer firmante de este trabajo, el Dr. Javier Robles-Valero, “Esto indica que estos genes pueden actuar como el famoso Dr. Jekyll and Mr. Hyde del libro de Stevenson dependiendo del tipo de células o tumor en el que se encuentren activos”. Sin embargo, el trabajo que se publica en Cancer Cell también ha permitido descubrir que estas dos funciones antagónicas de VAV1 se ejecutan a través de procesos moleculares diferentes. Esto sugiere que se podrán diseñar terapias específicas en un futuro inmediato que permitan inactivar las funciones protumorales o recrear las funciones antitumorales de este gen dependiendo del tipo de alteración del mismo en pacientes. Como apunta el Dr. Bustelo, “Esto nos hará replantear nuestros estudios en un futuro inmediato, puesto que hasta ahora todo el esfuerzo del laboratorio se había centrado en inhibir al Mr. Hyde que causa tumores. A partir de ahora también tendremos que ver a través de qué estrategias podremos mantener o volver al Dr. Jekyll antitumoral cuerdo todo el tiempo”. Apoyo al trabajo Este trabajo representó un tour de force de casi seis años en los que colaboraron investigadores españoles traslacionales y clínicos pertenecientes al CIBERONC, el Centro de Investigación del Cáncer de Salamanca, la Universidad de Salamanca, el CSIC, el Institut del Mar d’Investigacions Mèdiques de Barcelona y el Hospital Sant Joan de Déu de Esplugues del Llobregat. Como apunta el Dr. Bustelo, “Este trabajo es un buen ejemplo de cómo investigadores de distintos ámbitos pueden trabajar en común para abordar de forma efectiva un problema de relevancia biológica y clínica. En este sentido, el hecho de pertenecer al CIBERONC ha facilitado muy mucho este trabajo colaborativo”. La realización del trabajo fue posible gracias a financiación recibida desde el Ministerio de Economía y Competitividad, la Junta de Castilla y León, la Worldwide Cancer Research Foundation del Reino Unido, la Fundación Ramón Areces y la Asociación Española de Investigación contra el Cáncer. Fuente: Jano On Line |
Abuso de psicofármacos: una de cada tres argentinas toma tranquilizantes
Un estudio de la Sedronar reveló que casi 3 millones de argentinos de entre 12 y 65 años recurren a estos medicamentos para dormir, bajar la ansiedad o “disimular” una angustia.
Para dormir bien, calmar la ansiedad o “disimular” una angustia. Consumir psicofármacos se ha vuelto algo común entre los argentinos. Los medicamentos tranquilizantes, ansiolíticos y antidepresivos están en el botiquín familiar y se toman como si fueran aspirinas, sin advertir sus efectos adversos ni la adicción que generan.
Lo corroboran las estadísticas: según el Estudio de Consumo de Sustancias Psicoactivas realizado por la Sedronar entre 2016 y 2017, el 15% de la población de entre 12 y 65 años consume psicofármacos con o sin prescripción médica; esto es, casi tres millones de argentinos. “El consumo de este tipo de medicamentos es alto en la población urbana de nuestro país y aumenta con la edad, alcanzando el 26,4% entre los 50 y los 65 años en el caso de los tranquilizantes”, le dijo a PERFIL Verónica Brasesco, directora del Observatorio Argentino de Drogas.
El estudio de la Sedronar también encontró que la modalidad de uso es mayor en mujeres (17,6%) que en los varones (12,8%). “El psicofármaco es la única sustancia en la que hay una mayor prevalencia de consumo en mujeres, específicamente todos los que son antidepresivos”, agregó Brasesco. Entre los 35 y los 49 años, el 19,3% de las mujeres consumió tranquilizantes o ansiolíticos alguna vez en la vida y entre los 50 y los 65 la prevalencia llega al 35%. En tanto, el 4% usó estimulantes o antidepresivos. “Es alto el consumo en mujeres entre los 20 y los 50 años, cuando empieza la necesidad de una alta performance: estudiar, trabajar, tener hijos. Es una especie de ‘muleta química’ para aguantar el ritmo”.
Entre quienes refirieron haber consumido tranquilizantes o ansiolíticos alguna vez en la vida, la mayor parte pertenece al grupo de las benzodiacepinas, que actúan sobre el sistema nervioso central y tienen efectos sedantes, hipnóticos, ansiolíticos, anticonvulsivos y miorrelajantes. En mayor medida clonazepam (55,6%), alprazolam (30,2%) y diazepam (15,4%). Según datos de la consultora especializada IMS Health Argentina, es uno de los países con mayor consumo per cápita de clonazepam del mundo. En 2014 se vendieron más de un millón de unidades por día, 143% más que en 2004.
Dependencia
Para Brasesco, la funcionalidad del psicofármaco en la adolescencia y en la edad adulta es distinta. En los jóvenes prevalece el uso con fines recreativos, es la llamada “jarra loca” donde se mezclan pastillas y alcohol. “Es un consumo de alto riesgo para la salud porque se combina con otras sustancias”, señaló Brasesco.
En cambio, en los adultos los psicofármacos se utilizan para combatir situaciones cotidianas estresantes, de tensión o de incertidumbre. Muchas veces se buscan soluciones inmediatas a problemas con la ilusión de que son “pastillas mágicas”. “Se medicalizan los ciclos vitales: la menopausia en la mujer, todo lo que es el síndrome de nido vacío, la soledad. Esto tiene que ver con la vida en las grandes urbes”.
Las benzodiacepinas suelen generar dependencia y tolerancia, por eso los especialistas aconsejan no consumirlas por más de tres meses. “Son altamente adictivas. Salir del consumo, abandonarlo, es bien complicado”, advirtió Brasesco. Además, pueden producir somnolencia, irritabilidad, disminución de los reflejos y demencia. Por eso se deben consumir bajo prescripción médica.
El estudio de la Sedronar halló que el 21% de los que consumieron tranquilizantes alguna vez en la vida lo hicieron sin prescripción médica o iniciaron el consumo por indicación del médico y luego continuaron por su cuenta. Entre quienes sí tenían indicación médica (78%), en el 49% de los casos fue un médico generalista quien había recetado el tranquilizante y en un 37,2% un médico psiquiatra.
“Hay que hacer un gran trabajo con los médicos, por esto de que en ocasiones reproducen la receta de psicofármacos por años y luego hay un alto porcentaje de gente mayor con adicción a la sustancia. Para eso, firmamos un convenio con PAMI y queremos trabajar con todo lo que tiene que ver con medicalización de la vejez”. concluyó Brasesco.
Crece el consumo de marihuana, cocaína y alcohol
El Estudio de Consumo de Sustancias Psicoactivas en Población General fue realizado por la Sedronar entre 2016 y 2017. El informe, que encuestó a 20.658 personas de entre 12 y 65 años, representantes de una población total de 18.960.593 personas, arrojó datos alarmantes en torno a la situación de consumo de drogas y alcohol en todo el país. Entre los principales resultados, muchos de los cuales fueron presentados por el presidente Mauricio Macri a mitad de año, se halló que la marihuana es la droga ilícita de mayor consumo en el país: el 7,8% de la población declaró su uso en el último año. Sin embargo, son los varones y los jóvenes comprendidos entre los 18 y los 24 años los que presentan mayores tasas de consumo.
En tanto, el 5,3% de la población de entre 12 y 65 años consumió cocaína alguna vez en su vida, lo que implica un incremento del 100% con respecto al estudio de 2010. Por su parte, el consumo actual de alcohol se encuentra presente en el 53% de la población y en mayor medida en los varones. Entre los 18 y los 24 años se observa la tasa más elevada, con el 62% y entre los menores, la más baja con el 34,7%.
| Un uso naturalizado y en aumento | ||
| Se han ido instalando en la cultura los fármacos no como opción terapéutica sino como los que “resuelven” los problemas y angustias que conlleva vivir. Los medicamentos se han convertido en objetos que “garantizan la felicidad y el bienestar de la vida”. | ||
|
||
| La mayoría (66%) de los usuarios obtiene los tranquilizantes sin receta médica. Esta ingesta, combinada con bebidas alcohólicas, ocupa el segundo lugar entre los motivos de consulta por intoxicaciones, con el 11%. El abuso en el género femenino está ligado predominantemente a crisis depresivas o situaciones de descontrol emotivo. Y en el adolescente, vinculado con la búsqueda de sensaciones placenteras o de evasión y muchas veces constituido por la droga de iniciación. Los jóvenes han sido socializados en el consumo como modo de satisfacción de sus deseos y necesidades. No se trata sólo de fenómenos dopaminérgicos sino una resultante de la interacción dinámica de los cambios: físicos, psíquicos, intelectuales, socioambientales y espirituales, desde una visión integral y no reduccionista de la persona humana. La subjetividad anclada en la lógica del consumo favorece modalidades adictivas, satisfacción pulsional inmediata y desinvestidura del pensamiento y la palabra, con los consecuentes riesgos del incremento de las conductas violentas. Desde el punto de vista de políticas de salud, es importante recordar que el balance apropiado para una regulación efectiva del uso de los medicamentos es responsabilidad de los organismos regulatorios del Estado. Desde el punto de vista médico es fundamental subrayar la importancia del uso racional de los psicofármacos y recordar que no es la única alternativa para mitigar el sufrimiento humano.
* Director de Psiquiatría y Salud Mental del Instituto de Neurociencias Buenos Aires (Ineba). |
Fuente: Perfil
Lo más visto
- Covishield, la vacuna que India lanzó con Oxford-AstraZeneca
- El gobierno establece los requisitos para la producción de cannabis medicinal
- Anmat aprobó en el país la primera vacuna que protege contra el dengue
- Comunicación de Novo Nordisk: Diferencias en la indicación de Victoza® y Saxenda®
- Ibupirac declarado apto para celíacos