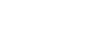Requisitos, exigencias y clasificación para la producción, registro en el REM, autorización y vigilancia de medicamentos de terapia avanzada
Disposición N°179/2018
Ciudad de Buenos Aires, 18/09/2018
VISTO la Ley Nº 16.643, sus Decretos Reglamentarios Nros. 9763/64, 150/92 (t.o.1993) y los Decretos Nros. 1490/92 y 341/92, Disposición ANMAT7075/05 y el Ex-2018—31030676-APN-DECBR#ANMAT del Registro de esta Administración Nacional de Medicamentos, Alimentos y TecnologíaMédica; y
CONSIDERANDO
Que el artículo 1° de la Ley 16463 establece que “quedan sometidos a la presente ley y a los reglamentos que en su consecuencia se dicten, la importación, exportación, producción, elaboración, fraccionamiento, comercialización o depósito en jurisdicción nacional o con destino al comercio interprovincial de las drogas, productos químicos, reactivos, formas farmacéuticas, medicamentos, elementos de diagnóstico, y todo otro producto de uso y aplicación en medicina humana y las personas de existencia visible o ideal que intervengan en dichas actividades”.
Que el artículo 20 de la citada ley establece que las actividades mencionadas sólo podrán realizarse previa autorización y bajo el contralor de la autoridad sanitaria, en establecimientos por ella habilitados y bajo la dirección técnica del profesional universitario correspondiente; todo ello en las condiciones y dentro de las normas que establezca la reglamentación, atendiendo a las características particulares de cada actividad y a razonables garantías técnicas en salvaguarda de la salud pública y de la economía del consumidor.
Que asimismo el artículo 3° del mencionado cuerpo legal prescribe que los productos comprendidos en la citada ley deberán reunir las condiciones establecidas en la Farmacopea Argentina, y en caso de no figurar en ella, las que surgen de los patrones internacionales y de los textos de reconocido valor científico, debiendo a la vez ser inscriptos por ante esta Administración Nacional de conformidad a lo establecido en el Decreto NO 150 /92 (T.O. 1993).
Que el artículo 1º del Decreto NO 9763/64, reglamentario de la Ley 16463, establece que el ejercicio del poder de policía sanitaria referido a las actividades indicadas en el artículo 1º de la mentada ley, y a las personas de existencia visible o ideal que intervengan en las mismas, se hará efectivo por el Ministerio de Asistencia Social y Salud Pública de la Nación (hoy Ministerio de Salud), en las jurisdicciones que allí se indican.
Que por su parte el Decreto NO 1490/92, crea esta Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT), como organismo descentralizado de la Administración Pública Nacional, con un régimen de autarquía financiera y económica, con jurisdicción en todo el territorio nacional, asumiendo dichas funciones.
Que en virtud del artículo 3º, inciso a) del mencionado decreto, esta Administración Nacional tiene competencia, entre otras materias, en todo lo referente al control y fiscalización sobre la sanidad y la calidad de las drogas, productos químicos, reactivos, formas farmacéuticas, medicamentos, elementos de diagnóstico, materiales y tecnologías biomédicas y todo otro producto de uso y aplicación en medicina humana.
Que esta Administración Nacional es la autoridad reguladora de medicamentos, y está facultada para otorgar su registro sanitario, de acuerdo a los requisitos y procedimientos establecidos en cada caso.
Que por Disposición 7075/11 la ANMAT estableció los requisitos que deben cumplimentar los solicitantes que pretendan inscribir en el registro REM de la ANMAT los medicamentos biológicos de uso humano.
Que las Terapias avanzadas como la terapia génica, la terapia celular somática y la ingeniería tisular constituye un campo emergente de las ciencias biomédicas ofreciendo nuevas oportunidades para el tratamiento de enfermedades o disfunciones corporales humanas.
Que los medicamentos de terapia avanzada destinados al tratamiento o prevención de enfermedades humanas o bien para ser empleados para su administración a los seres humanos para restaurar, corregir o modificar funciones fisiológicas por ejercer principalmente una acción farmacológica, inmunológica o metabólica se encuentran comprendidos en la definición de medicamentos biológicos, debiendo por lo expuesto cumplimentar los requerimientos establecidos para estos productos.
Que no obstante lo expuesto precedentemente, dada la complejidad de los medicamentos de terapia avanzada, deviene necesario dictar normas específicas que establezcan los requisitos científicos y técnicos y exigencias particulares aplicables a la producción, registro y autorización de comercialización y vigilancia de estos productos biológicos, con el fin de acreditar en forma fehaciente su calidad, eficacia y seguridad.
Que en tal sentido, y en términos de convergencia regulatoria, la Dirección de Evaluación y Control de Biológicos y Radiofármacos del INAME realizó un estudio de los criterios generales internacionalmente aceptados respecto al marco regulatorio general y requerimientos específicos establecidos para la producción, autorización de comercialización y vigilancia de medicamentos de terapia avanzada, a fin de ser considerados e incorporarlos a la normativa ANMAT vigente, en el contexto del marco regulatorio nacional.
Que la Dirección de Evaluación y Control de Biológicos y Radiofármacos del INAME y la Dirección General de Asuntos Jurídicos han tomado la intervención de su competencia.
Que se actúa en virtud de las facultades conferidas por los Decretos 1490/92 y 101 de fecha 16 de diciembre de 2015.
Por ello,
EL ADMINISTRADOR NACIONAL DE LA ADMINISTRACIÓN NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGIA MÉDICA
DISPONE:
ARTICULO 1°.- Establécense los requisitos, exigencias y clasificación para la producción, registro en el REM, autorización y vigilancia de Medicamentos de terapia avanzada que sean producidos o preparados industrialmente o en cuya fabricación intervenga un proceso industrial.
ARTICULO 2°.- A los efectos de la presente disposición, entiéndase como:
Medicamentos de terapias avanzada: a los siguientes medicamentos biológicos para uso humano:
— un medicamento de terapia génica
— un medicamento de terapia celular somática,
— un producto de ingeniería tisular
Medicamento de terapia génica: es un medicamento biológico con las características siguientes:
a. incluye un principio activo que contiene un ácido nucleico recombinante, o está constituido por él, utilizado en seres humanos, o administrado a los mismos, con objeto de regular, reparar, sustituir, añadir o eliminar una secuencia génica;
b. su efecto terapéutico, profiláctico o diagnóstico depende directamente de la secuencia del ácido nucleico recombinante que contenga, o del producto de la expresión genética de dicha secuencia.
Los medicamentos de terapia génica no incluyen las vacunas contra enfermedades infecciosas.”
Medicamento de terapia celular somática: es un medicamento biológico con las características siguientes:
a. contiene células o tejidos, o está constituido por ellos, que han sido objeto de manipulación sustancial de modo que se hayan alterado sus características biológicas, funciones fisiológicas o propiedades estructurales pertinentes para el uso clínico previsto, o por células o tejidos que no se pretende destinar a la misma función esencial en el receptor y en el donante; b. se presenta con propiedades para ser usado por seres humanos, o administrado a los mismos, con objeto de tratar, prevenir o diagnosticar una enfermedad mediante la acción farmacológica, inmunológica o metabólica de sus células o tejidos.
A efectos de la letra a), no se considerarán manipulaciones sustanciales las enumeradas en Anexo I (IF-2018-44144428-APN-DECBR#ANMAT) de la presente disposición y que forma parte integral de la misma.
Producto de ingeniería tisular: se entenderá aquel producto biológico:
a. que contiene o está formado por células o tejidos manipulados por ingeniería, y
b. del que se alega que tiene propiedades, se emplea o se administra a las personas para regenerar, restaurar o reemplazar un tejido humano.
Un producto de ingeniería tisular podrá contener células o tejidos de origen humano, animal, o ambos. Las células o tejidos podrán ser viables o no. Podrá también contener otras sustancias, como productos celulares, biomoléculas, biomateriales, sustancias químicas, soportes o matrices.
Células o tejidos manipulados por ingeniería: se considerarán células o tejidos manipulados por ingeniería a aquellos que cumplen con al menos una de las condiciones siguientes: las células o tejidos han sido sometidos a manipulación sustancial, de modo que se logren las características biológicas, funciones fisiológicas o propiedades estructurales pertinentes para la regeneración, reparación o sustitución pretendidas. Las manipulaciones enumeradas en particular en el Anexo I (IF-2018-44144428-APN-DECBR#ANMAT) no se consideran sustanciales, las células o tejidos no están destinados a emplearse para la misma función o funciones esenciales en el receptor y en el donante.
Las células o tejidos están destinados a implantarse en un nicho diferente de aquel a partir del cual fueron obtenidos.
Medicamento combinado de terapia avanzada: se entenderá el medicamento de terapia avanzada que cumple las siguientes condiciones:
— tiene que incorporar, como parte integrante del mismo, uno o más productos médicos, o uno o más productos médicos implantables activos; y
— su parte celular o tisular tiene que contener células o tejidos viables, o su parte celular o tisular que contenga células o tejidos no viables tiene que poder ejercer en el organismo humano una acción que pueda considerarse fundamental respecto de la de los productos médicos mencionados.
ARTICULO 3°.- Quedarán excluidos de la presente definición los productos que contienen o están formados exclusivamente por células y/o tejidos humanos o animales no viables, que no contengan células o tejidos viables y que no ejerzan principalmente una acción farmacológica, inmunológica o metabólica.
ARTICULO 4°.- Cuando un producto contenga células o tejidos viables, la acción farmacológica, inmunológica o metabólica de dichas células o tejidos se considerará como el modo de acción principal del producto.
ARTICULO 5°.-. Se considerará que un medicamento de terapia avanzada que contenga células o tejidos tanto autólogos (procedentes del propio paciente) como alogénicos (procedentes de otra persona) es para uso alogénico.
ARTICULO 6°.- Un medicamento que pueda corresponder tanto a la definición de producto de ingeniería tisular como a la de medicamento de terapia celular somática se considerará producto de ingeniería tisular.
ARTICULO 7°.- Un medicamento que pueda corresponder a la definición de: medicamento de terapia celular somática o de producto de ingeniería tisular, y medicamento de terapia génica, se considerará medicamento de terapia génica.
ARTICULO 8°.- Los productos fabricados exclusivamente con materiales no viables que actúan principalmente por medios físicos, no pueden por definición ser considerados medicamentos y por lo tanto no pueden ser considerados medicamentos de terapia avanzada.
ARTICULO 9°.- Cuando un producto no cumpla las condiciones estipuladas en las definiciones anteriores, no se considerará medicamento de terapia avanzada. Un ejemplo sería el caso de células o tejidos para implante que no hayan sido objeto de una manipulación sustancial y que se vayan a utilizar con la misma función esencial en donante y receptor.
ARTICULO 10.- Los medicamentos de terapia avanzada quedan sometidos a los mismos principios reglamentarios aplicables a los medicamentos obtenidos por biotecnología. No obstante, dada la naturaleza de estos productos resulta necesario establecer los requisitos técnicos, tales como requerimientos relacionados con los aspectos de calidad, preclínicos y clínicos necesarios para demostrar la calidad, seguridad y eficacia del producto. La ANMAT establecerá la reglamentación o guías específicas a tal fin, sobre la base de lineamientos internacionalmente reconocidos.
ARTICULO 11.- Los requisitos técnicos específicos aludidos en el artículo precedente, deberán ser comprendidos como requerimientos complementarios y, en su caso adicionales, a los establecidos para medicamentos en general y para medicamentos biológicos en particular.
ARTICULO 12.- Cuando un medicamento de terapia avanzada contenga células y tejidos de origen humano, las etapas de donación, obtención y el análisis/ verificación, quedan sujetas a la reglamentación vigente establecida por la Autoridad Competente en esa materia).
ARTICULO 13.- En lo que se refiere a la donación de células o tejidos humanos, deben respetarse los principios de anonimato tanto del donante como del receptor, el altruismo del donante y la solidaridad entre el donante y el receptor.
Las células o los tejidos que contengan los medicamentos de terapia avanzada deben obtenerse mediante donación voluntaria y no remunerada.
ARTICULO 14.- Los estudios de investigación clínica con medicamentos de terapia avanzada deben realizarse ajustándose a los principios fundamentales y los requisitos éticos establecidos en la normativa vigente, debiendo cumplimentar asimismo con los requerimientos de buenas prácticas clínicas en la realización de ensayos clínicos de medicamentos de uso humano. así como los requisitos para autorizar la fabricación o importación de dichos productos.
ARTICULO 15.- La fabricación/preparación de medicamentos de terapia avanzada debe ajustarse a los requerimientos generales de buenas prácticas de fabricación vigentes aplicables a medicamentos de uso humano y medicamentos/productos en investigación clínica y a los específicos aplicables a medicamentos de origen biológico.
ARTICULO 16.- La ANMAT establecerá, de ser necesario guías que contemplen aspectos particulares de la producción y control de estos productos.
ARTICULO 17.- Las solicitudes de autorización de comercialización de medicamentos de terapia avanzada, deberán cumplir los requisitos y formatos establecidos en la Disposición 7075/11 o en las que en su consecuencia se dicten o reemplacen.
ARTICULO 18.- La ANMAT establecerá, en caso de considerarlo necesario, guías que contemplen requisitos específicos para los medicamentos de terapia avanzada en relación a los aspectos de calidad, preclínicos y clínicos a ser evaluados para su inscripción en el REM.
ARTICULO 19.- Debido a la naturaleza específica de los medicamentos de terapia avanzada, la ANMAT podrá requerir un análisis del riesgo para determinar la extensión de los datos de calidad, no-clínicos y clínicos que deben incluirse en la solicitud de autorización de comercialización, en los términos de la información científico-técnica relacionada con la calidad, seguridad y eficacia de los medicamentos de terapia avanzada.
El análisis del riesgo podrá cubrir todo el proceso. Los factores de riesgo que deben estar incluidos son: el origen de las células (autólogo, alogénico, xenogénico), la capacidad de proliferación o diferenciación y de iniciar una respuesta inmunitaria, el nivel de manipulación celular, la combinación de células con moléculas bioactivas o materiales estructurales, la naturaleza de los medicamentos de terapia génica, el grado de capacidad replicativa de los virus o microorganismos utilizados in vivo, el nivel de integración de los genes o las secuencias de ácidos nucleicos en el genoma, la funcionalidad a largo plazo, el riesgo de carcinogenicidad y el modo de administración o uso. También pueden tenerse en cuenta para el análisis de riesgo la experiencia o los datos no-clínicos y clínicos disponibles y pertinentes relativos a otros medicamentos de terapia avanzada relacionados. Cualquier desvío a estos requisitos, deberá justificarse científicamente en el expediente de solicitud.
ARTICULO 20.- Cuando se aplique el análisis del riesgo citado en el artículo precedente, deberá incluirse y describirse la metodología seguida, la naturaleza de los riesgos identificados y las implicaciones del planteamiento basado en el análisis de riesgo para el programa de desarrollo y evaluación, y se describirá cualquier desviación de los requisitos establecidos en la normativa vigente que resulte del análisis del riesgo.
ARTICULO 21.- Cuando un medicamento de terapia avanzada incorpore un producto médico o un producto médico implantable activo, se considerará un medicamento combinado de terapia avanzada y la totalidad del producto será objeto de evaluación global por parte de la ANMAT.
ARTICULO 22.- El producto médico o producto medico implantable activo citado en el artículo precedente, deberá cumplir, los requisitos esenciales establecidos en la normativa vigente aplicable a productos médicos a fin de garantizar el nivel adecuado de calidad y de seguridad.
ARTICULO 23.- En las solicitudes de autorización de un medicamento de terapia avanzada que contenga productos médicos, biomateriales, soportes o matrices, deberá presentarse una descripción de sus características físicas, de su rendimiento y de sus métodos de diseño, de conformidad con lo establecido en la normativa vigente para estos productos, incluyendo la prueba de conformidad y los resultados de la evaluación de la parte del producto médico o de la parte del producto médico implantable activo, esto último, de encontrarse disponible. En caso de no estar disponible, se dará intervención a la Dirección Nacional de Productos médicos para la evaluación de la parte del producto médico contenido en el medicamento de terapia avanzada combinado.
ARTICULO 24.- Considerando la importancia del seguimiento de la eficacia y las reacciones adversas de los medicamentos de terapia de avanzada, el solicitante debe presentar en la solicitud de autorización de comercialización el Plan de gestión del riesgo para hacer frente a los riesgos de forma tal de contar con un sistema apropiado que le permita detectar, caracterizar, prevenir o minimizar los riesgos inherentes a los medicamentos de terapia avanzada, que incluya una evaluación de la eficacia del propio sistema, o que el titular de la autorización de comercialización lleve a cabo estudios específicos posteriores a la comercialización y los presente para su revisión a la ANMAT. La evaluación de la efectividad de cualquier sistema de gestión del riesgo y de los resultados de cualesquiera estudios realizados se incorporará a los informes periódicos actualizados en materia de seguridad
ARTICULO 25.- Dada la naturaleza y origen de estos productos, resulta esencial contar con un sistema que permita la trazabilidad completa del paciente, del producto y de sus materias primas, para monitorizar la seguridad de los medicamentos de terapia avanzada.
En esta sentido el titular de la autorización de comercialización de un medicamento de terapia avanzada establecerá y mantendrá un sistema de trazabilidad de forma tal de garantizar la trazabilidad (capacidad de rastreo y reconstrucción) de cada producto y de sus materias primas, materiales de partida, incluidas todas las sustancias que entren en contacto con los tejidos o células que contenga, a lo largo del abastecimiento, la producción/preparación, el acondicionamiento y rotulado, el almacenamiento, el transporte y el suministro al hospital, la institución o centro en que vaya a usarse.
ARTICULO 26.- El productor deberá garantizar que el hospital, la institución o el centro en que vaya a usarse el medicamento de terapia avanzada haya establecido y mantenga un sistema que permita la trazabilidad del paciente y del producto. El sistema será lo suficientemente detallado para permitir vincular cada producto al paciente que lo recibió y viceversa. La característica del sistema deberá ser presentado y explicado al momento de solicitar la autorización del producto.
ARTICULO 27.- Cuando un medicamento de terapia avanzada contenga células o tejidos humanos, el titular de la autorización de comercialización, así como el hospital, la institución o centro en que vaya a usarse, deberán asegurar que los sistemas de trazabilidad establecidos de conformidad con la presente normativa sean coherentes, compatibles y complementarios con los establecidos en la normativa establecida por la autoridad de aplicación en lo relativo a la donación, obtención y análisis/verificación de células y tejidos humanos.
ARTICULO 28.- El titular de la autorización de comercialización conservará los datos mencionados en el artículo precedente, como mínimo, treinta años después de la fecha de caducidad del producto. El tiempo podrá ser superior en caso de que la autorización de comercialización así lo establezca.
ARTICULO 29.- El sistema de trazabilidad debe respetar asimismo lo previsto en las normativas vigentes relacionadas con la protección de las personas físicas en lo que respecta al tratamiento de datos personales y a la libre circulación de estos datos.
ARTICULO 30.- El rotulado del envase secundario y primario de un medicamento de terapia avanzada, deberá cumplimentar los requerimientos establecidos en la reglamentación vigente. En aquellos casos en los cuales no sean distribuidos con un envase secundario, los datos completos deberán estar incluidos en el material de acondicionamiento primario.
ARTICULO 31.- Acondicionamiento primario especial. Sin perjuicio de lo expuesto en el artículo precedente, el material de acondicionamiento primario deberá contener la siguiente información:
a) el código único de cada donación y cada producto.
b) en el caso de medicamentos de terapia avanzada de uso autólogo, el identificante único del paciente y la mención “Solo para uso autólogo”.
ARTICULO 32.- En relación al prospecto que acompaña a los medicamentos de terapia avanzada, el mismo será redactado considerando la información contenida en el resumen de características del producto, y contendrá la información descripta en el Anexo II (ANEXO II-IF-2018-44144886-APN-DECBR#ANMAT) de la presente disposición y que forma parte integral de la misma.
ARTÍCULO 33.- El incumplimiento de la presente Disposición hará pasible a los infractores de las sanciones previstas en la Ley 16.463, las normas dictadas en su consecuencia o las que en el futuro las modifiquen o sustituyan.
ARTICULO 34.- La presente disposición entrará en vigencia a partir del día siguiente a su publicación en el Boletín Oficial.
ARTICULO 35.– Regístrese. Dése a la Dirección Nacional del Registro Oficial para su publicación. Comuníquese a las Autoridades Sanitarias Provinciales, a la del Gobierno de la Ciudad Autónoma de Buenos Aires y a la Dirección General de Aduanas – Administración Federal de Ingresos Públicos (AFIP). Notifíquese a las Cámaras de Especialidades Medicinales (CILFA, CAEME, COOPERALA, CAPGEN, CAPEMVeL, SAFYBI), Confederación Médica de la República Argentina (COMRA) y la Confederación Farmacéutica Argentina (COFA). Dése al Instituto Nacional de Medicamentos y a la Dirección de Relaciones Institucionales y Regulación Publicitaria de esta Administración Nacional. Cumplido archívese. Carlos Alberto Chiale
NOTA: El/los Anexo/s que integra/n este(a) Disposición se publican en la edición web del BORA -www.boletinoficial.gob.ar-
e. 20/09/2018 N° 69924/18 v. 20/09/2018
Fecha de publicación 20/09/2018
El antifúngico ciclopirox puede ser útil en la porfiria eritropoyética
El fármaco antifúngico ciclopirox ha demostrado mejorar los síntomas de la porfiria eritropoyética congénita en el modelo murino de la enfermedad. Así lo revela un estudio realizado por investigadores del CIC bioGUNE y de la empresa biotecnológica Atlas Molecular Pharma, cuyas conclusiones se publican en Science Translational Medicine.
La porfiria eritropoyética congénita es una enfermedad rara que afecta a menos de una persona por millón de habitantes. Esta enfermedad se produce por una deficiencia en la actividad de la enzima uroporfirinógeno III sintasa (UROIIIS), que actúa en la ruta de síntesis del grupo hemo, lo que provoca una reducción de la vida útil de los glóbulos rojos (anemia) y una extrema fotosensibilidad, formación de ampollas y aumento de las infecciones bacterianas en la piel. Los síntomas pueden aparecer durante la infancia o, en los casos menos graves, en la edad adulta. Los tratamientos existentes solo alivian la sintomatología sin que exista ningún tipo de terapia efectiva.
Con ayuda de una plataforma de cribado de moléculas para el descubrimiento y validación de chaperonas farmacológicas diseñada por la biotecnológica, analizaron varios miles de fármacos y pequeñas moléculas escogidos por su capacidad para interactuar con la enzima UROIIIS. Así, estos investigadores han descubierto que el fármaco ciclopirox podría reposicionarse como tratamiento de la porfiria eritropoyética congénita. Al ser una molécula ya existente para el tratamiento de otras enfermedades, el compuesto está aprobado por las agencias reguladoras de medicamentos, lo que facilitará el complejo proceso de su desarrollo para la porfiria.
El hallazgo es fruto de la labor desarrollada durante la última década en el laboratorio de Estabilidad de Proteínas y Enfermedades Congénitas de CIC bioGUNE por el equipo de Oscar Millet. El laboratorio está enfocado en entender cómo algunos cambios en la estructura de determinadas proteínas produce su inestabilización, y en última instancia desencadena un proceso patológico. “Entender el mecanismo molecular de la enfermedad ha permitido diseñar una terapia basada en chaperonas farmacológicas, que son moléculas que se unen a la proteína defectuosa, corrigiendo su problema de estabilidad y revertiendo sus efectos patogénicos”, explica Millet.
El éxito de este reposicionamiento radica en la sinergia entre un equipo investigador altamente cualificado y las infraestructuras de primer nivel existentes en CIC bioGUNE. Merece la pena destacar las inversiones realizadas en el animalario, que ha albergado los experimentos con modelos animales de porfiria eritropoyética congénita bajo la supervisión de Joaquín Castilla y en la plataforma de resonancia magnética nuclear, que ha permitido obtener información inequívoca acerca del mecanismo de acción del fármaco.
El estudio es un paso más hacia el inicio de ensayos clínicos con pacientes en un futuro cercano. Supone la acreditación formal de que esta molécula tiene la actividad farmacológica adecuada tanto in vitro como in vivo, habiéndose demostrado eficacia en modelos murinos de la enfermedad.
Fuente: Diario Médico / COFA
FUNCEI inaugura este mes el ciclo de charlas online e interactivas, Stamboulian Talks
Se trata de una excelente oportunidad para compaginar las agendas apretadas de los profesionales de la salud con sus necesidades de formación continua. Este ciclo de charlas está dirigido a profesionales médicos y sanitarios y estará impartido por prestigiosos médicos especialistas de distintas áreas, muchos de ellos colaboradores del doctor Daniel Stamboulian.
La sesión inaugural será el 20 de septiembre a las 12:30 y estará a cargo del Dr. Marcelo Laurido, quien hablará sobre "Introducción a las hepatitis virales: impacto sanitario". A continuación, a las 13 hs, el Dr. Pablo Elmassian hablará sobre "Medicina del viajero".
Para participar de la sesión inaugural, basta inscribirse haciendo click en este formulario online. Las personas interesadas recibirán un enlace mediante el cual podrán acceder el día del taller desde cualquier dispositivo y de forma gratuita.
Todas las sesiones del ciclo Stamboulian Talks tendrán un formato de 1 hora de duración con 2 charlas cada sesión. Las sesiones intercalarán temas de clínica médica con pediatría. Si bien están destinadas a un público profesional, las charlas tendrán un estilo ameno y una duración de 20 minutos cada una y, al término de la misma, se dejarán 10 minutos para responder a las preguntas que envíen los participantes por el chat.
Con aval científico
Stamboulian Talks cuenta con el apoyo de distintas instituciones: la Sociedad Argentina de Infectología, la Sociedad Argentina de Pediatría, la Sociedad Argentina de Cardiología, la Sociedad Argentina de Nutrición, la Sociedad Argentina de Nefrología, la Sociedad de Medicina Interna de Buenos Aires, la Sociedad Argentina de Gerontología y Geriatría, la Sociedad Paraguaya de Infectología, la Sociedad de Infectología de Tucumán, el International Life Sciences Institute de Argentina (ILSI), Paideia, el Grupo Asesor de Control de Infecciones y Epidemiología y Fighting Infectious Diseases in Emerging Countries (FIDEC).
Medio ambiente y salud: Los insectos introducen contaminación plástica en la cadena alimentaria
Un nuevo estudio en la Universidad de Reading descubrió que pequeños fragmentos de plástico penetran en insectos voladores que ponen sus huevos en el agua, y que pueden pasar de las larvas a la forma adulta.
Los científicos descubrieron que los microplásticos consumidos por las larvas permanecen invariablemente en el mosquito a través de la metamorfosis a una pupa que no está alimentándose y luego a los adultos. Insectos voladores como éstos son devorados por pájaros y murciélagos, lo que proporciona un potencial nuevo camino para que los plásticos ingresen a la cadena alimenticia.
La bióloga Amanda Callaghan, autora principal del estudio, declaró en un comunicado: “Se ha prestado mucha atención recientemente a los plásticos que contaminan nuestros océanos, pero esta investigación revela que también está en nuestros cielos.
“Esta es una investigación reveladora, que nos ha demostrado por primera vez que los microplásticos son capaces de atravesar varias etapas de la vida en insectos voladores, lo que les permite contaminar todo tipo de criaturas vivas que normalmente no estarían expuestas a ellas. Es una realidad impactante que el plástico esté contaminando casi todos los rincones del medioambiente y sus ecosistemas “.
Los microplásticos pueden originarse a partir de la contaminación plástica, que demora cientos de años en descomponerse en el medio ambiente, y se ha descubierto que está muy extendida en los océanos y en el agua dulce de todo el mundo. También se liberan directamente en el agua residual como diminutas perlas en muchos productos cosméticos. Estos son consumidos por organismos acuáticos y se transfieren a través de la cadena alimenticia a peces y otras criaturas.
El nuevo estudio, publicado en Biology Letters, muestra por primera vez que los microplásticos se pueden transmitir entre las etapas de la vida de las criaturas que viven en el agua antes de pasar a un ambiente terrestre.
La estudiante de doctorado Rana Al-Jaibachi alimentó con microperlas de plástico fluorescente a las larvas de mosquito y monitoreó su destino a lo largo de su ciclo de vida. Ella usó microscopios para examinar si los microplásticos se habían transferido de alimentar las etapas larvales a la etapa de pupa sin alimentación y al insecto adulto.
Fuente: Europa Press / COFA
La presión arterial tiene base hereditaria: Estudio con más de un millón de participantes
|
El estudio genético sobre presión arterial más extenso hasta la fecha recopila más de mil regiones implicadas, lo que podría impulsar el desarrollo de medidas preventivas y nuevos tratamientos. |
||
|
|
||
| Un estudio que ha involucrado a más de un millón de participantes desvela 500 nuevas regiones genéticas que influyen en la presión arterial. El trabajo se publica en Nature Genetics y tiene a Mark Caulfield, de la Universidad Queen Mary de Londres, y a Paul Elliott, del Imperial College London, como autores principales.
Con estos resultados, las regiones de genes vinculadas a la presión arterial se elevan a más de mil; además, explican casi un tercio de los factores heredados que influyen en los niveles tensionales. También aclara el papel de estos genes, no solo en los vasos sanguíneos, sino en las glándulas suprarrenales y en la grasa corporal. El profesor Mark Caulfield, director del Centro Barts de Investigación Biomédica del Instituto Nacional británico NIHR, afirma: “Este es el avance más importante en la genética de la presión arterial hasta la fecha. Ahora sabemos que hay más de mil señales genéticas que influyen en nuestra presión arterial. Esto nos proporciona nuevos conocimientos sobre cómo nuestro organismo regula la presión arterial y revela varias nuevas oportunidades para el futuro desarrollo de medicamentos”. El profesor Roberto Elosua participa en el estudio. El estudio sugiere algunas dianas potenciales para desarrollar fármacos frente a la hipertensión y también algún que otro reposicionamiento de medicamentos prescritos para otras enfermedades. Por ejemplo, una de las regiones genéticas desveladas es el objetivo del fármaco antidiabético canagliflozina. También se ha constatado que ciertos genes implicados en la presión arterial lo están en otras patologías; es el caso de APOE y la enfermedad de Alzheimer. “Con esta información, podríamos calcular el nivel de riesgo genético de una persona para la presión arterial alta a lo largo de su vida. Adoptando un enfoque de medicina de precisión, los médicos podrían dirigir intervenciones tempranas de estilo de vida en aquellos con un riesgo genético alto, como perder peso, reducir el consumo de alcohol y hacer más ejercicio”. El profesor Paul Elliott, del Imperial College London, asegura que “identificar este tipo de rasgos genéticos nos ayudará cada vez más a dividir a los pacientes en grupos según su riesgo. Al identificar a los pacientes con el mayor riesgo subyacente, podemos ayudarlos a cambiar los factores de estilo de vida que los hacen más propensos a desarrollar enfermedades”, además de posibilitar abordajes específicos preventivos. Fuente: Diario Médico – España / COFA |
Un nuevo material permite la liberación controlada de medicamentos
Investigadores de la Unesp y de la Universidad de Francia combinan arcilla y polímero a escala nanométrica para crear una estructura que posibilita acarrear y liberar fármacos gradualmente.
Siendo ya utilizados en agricultura y en cosméticos, los minerales de la arcilla pueden ser aplicados en medicamentos como antiinflamatorios y quimioterápicos, para mejorar sus efectos.
Investigadores del Instituto de Química de la Universidad Estadual Paulista (Unesp), campus de Araraquara, y de la Universidad de Francia (Unifran) desarrollaron un nuevo material, a base de arcilla y de un polímero. La estructura permite acarrear y liberar fármacos de forma lenta y gradual. De esta manera, permite controlar la absorción de medicamentos por el organismo y evitar las oscilaciones de la concentración en el torrente sanguíneo.
El nuevo material fue desarrollado en el marco del INCT de Tecnologías Ecoeficientes Avanzadas en Productos Cimentos – uno de los INCTs financiados por la FAPESP en asociación con el Consejo Nacional de Desarrollo Científico y Tecnológico (CNPq) en el Estado de São Paulo. El proceso de obtención de la estructura fue descrito en un artículo publicado en la revista Applied Materials & Interfaces, de la American Chemical Society.
“Combinamos una arcilla comercial, llamada montmorillonita sódica, con un gel polimérico a escala nanométrica [de la billonésima parte del metro]. Con eso, conseguimos obtener un material que posibilite liberar una medicación paulatinamente, en las dosis y tasas más adecuadas, manteniendo la concentración ideal en la corriente sanguínea “, dijo Eduardo Molina, profesor de la Unifran y uno de los autores de la investigación, a la Agencia FAPESP.
Los investigadores incorporaron la montmorillonita sódica en una matriz flexible y transparente, compuesta por polióxido de etileno (PEO). Este material, con características de hidrogel, en forma de una red rígida tridimensional, es capaz de absorber volúmenes elevados de agua en sus intersticios, sin disolverse. Por lo tanto, se considera un excelente material para la liberación controlada de fármacos.
Sin embargo, el hidrogel permite la liberación de un fármaco muy rápidamente. Además, puede presentar un problema, llamado burst release – liberación inmediata -, donde una dosis alta de un medicamento se libera al principio y luego se mantiene a una determinada tasa. “El hidrogel a base de polióxido de etileno no permite obtener la liberación lenta y controlada del fármaco“, dijo Molina.
Una vez que la arcilla es conocida como un material impermeabilizante, los investigadores tuvieron la idea de tratar de combinarla con el hidrogel para verificar si el material podría constituirse en una barrera y permitir un control fino de la cantidad de fármaco liberado.
Para probar esta hipótesis, diferentes concentraciones de montmorillonita sódica se incorporaron en un hidrogel híbrido orgánico-inorgánico, llamado siloxano-poliéter o ureasil, por medio de un proceso llamado sol-gel.
Este método de preparación de materiales se basa en una serie de reacciones químicas, en las cuales ocurre la transformación de un líquido con partículas nanométricas en suspensión – el “sol” – en un gel.
La combinación de los dos materiales -la arcilla y el hidrogel polimérico- resultó en un nanocompuesto en el que se incorporó diclofenaco sódico durante la preparación del material. El fármaco es un antiinflamatorio, administrado por vía oral o por inyección, bastante utilizado para aliviar la hinchazón y el dolor generados, por ejemplo, por artritis, reumatismo, lesiones musculares, cirugías o gota.
Los análisis de las estructuras de los nanocompuestos, realizadas a través de diferentes técnicas de caracterización, revelaron que era posible distinguir claramente el hidrogel polimérico, la arcilla y el fármaco en los materiales.
En las pruebas de rendimiento del material en la liberación del diclofenaco, realizadas en laboratorio, en recipientes que simulan las condiciones biológicas, se constató que la arcilla fue esencial para controlar la forma en que el fármaco era liberado.
Al ajustar el porcentaje de arcilla utilizado en la preparación de los nanocompuestos, fue posible evitar que una dosis grande de diclofenaco sódico fuera liberada al principio, y que la liberación posterior ocurría de forma pausada y a una tasa constante y previsible.
“Conseguimos obtener un efecto, llamado difusión de barrera, que permitió controlar la cantidad de fármaco liberada de acuerdo con el tiempo”, explicó Molina.
Láminas nanométricas
Los investigadores constataron que, dependiendo de la cantidad de montmorillonita sódica incorporada en el hidrogel, la arcilla asume la forma de láminas nanométricas homogéneamente dispersas en el material. Estas láminas nanométricas de arcilla actuaron como una barrera física al paso de las moléculas de agua y del fármaco por los canales del hidrogel.
“Las láminas de arcilla formaron un laberinto en el interior del material, que retardó el movimiento e imprimió un determinado ritmo a la absorción de agua y a la liberación del diclofenaco sódico”, afirmó Molina.
En la evaluación de los investigadores, el nanocompuesto podría ser utilizado para revestir píldoras, por ejemplo, y actuar como un sistema de liberación de fármacos para tratamientos prolongados de artritis, migraña y dolor post-quirúrgico, entre otros.
El artículo “Highly controlled diffusion drug release from ureasil–poly(ethylene oxide)–Na+–montmorillonite hybrid hydrogel nanocomposites” (doi: 10.1021/acsami.8b04559), de Celso R. N. Jesus, Eduardo F. Molina, Sandra H. Pulcinelli e Celso V. Santilli, puede ser leído en la revista Applied Materials & Interfaces em pubs.acs.org/doi/10.1021/acsami.8b04559.
Fuente:
| Agencia FAPESP -Brasil /COFA |
El caparazón proteico del rotavirus encierra las claves de la infección
Investigadores de la Universidad Autónoma de Madrid (UAM), el Instituto de Salud Carlos III (ISCIII) y el Centro Nacional de Biotecnología (CNB) lograron medir las propiedades mecánicas de las múltiples capas proteicas que protegen al rotavirus. Los resultados, publicados en eLife, podrían abrir nuevas vías para el desarrollo de tratamientos frente a la infección por este tipo de virus, responsable de gran parte de las enfermedades diarreicas en la infancia desde su nacimiento hasta los cinco años.
Este estudio es el primero que detalla la interacción entre la función y las propiedades mecánicas de un virus de múltiples capas. Las partículas virales encierran su material genético en un caparazón proteico diseñado para proteger, transportar y liberar el genoma viral en la célula huésped.
Para conseguir esto, la estructura de las partículas virales debe ser lo suficientemente resistente como para proteger el genoma viral en entornos externos a la célula y resistir los ataques del sistema inmune del huésped, garantizando una infección exitosa. Muchos virus de ARN bicatenario rodean su genoma de una capa protéica característica que incorpora su propia maquinaria molecular para permitir que el genoma se replique y propague. Algunos de estos virus añaden capas de proteína adicionales que participan en funciones específicas. Por ejemplo, rotavirus ha concentrado toda la maquinaria necesaria para la interacción y la entrada en la célula diana en la capa más externa de su partícula viral.
La partícula completa de rotavirus está formada por tres capas de proteína independientes. “Esta partícula y partículas subvirales que contienen una o dos capas de proteína desempeñan diferentes papeles durante la infección”, explica el autor principal, Manuel Jiménez-Zaragoza, de la UAM. “Queríamos ver cómo contribuyen las interacciones entre las capas que definen estas diferentes partículas al ciclo de replicación del virus”, añade.
Tres capas de proteínas
Los autores aislaron cada una de las diferentes partículas y subparticulas virales de rotavirus, y las estudiaron mediante microscopía de fuerzas atómicas (AFM). Los resultados muestran la presencia de una fuerte interacción entre la delgada capa externa y la gruesa capa media de la partícula viral, que resulta crítica para la protección del virion infectivo.
Interacciones más débiles entre los componentes de la capa media y de estos con la capa interna permiten a esta gruesa capa realizar su papel como adaptador entre las capas interna y externa, y la dotan de la flexibilidad necesaria para permitir al virus replicar su genoma en las células anfitrionas, un proceso conocido como transcripción.
“Nuestros hallazgos revelan cómo las propiedades biofísicas de las tres capas proteicas se ajustan para permitir que el rotavirus infecte de forma eficiente las células del huésped”, apunta Pedro de Pablo, otro de los autores de la UAM. “Este trabajo aporta valiosa información e importantes dianas para el desarrollo de nuevas estrategias antivirales”, concluye.
Fuente: Jano On Line / COFA
La SAP recomienda 'cero alcohol' hasta los 18 años
En nuestro país, el consumo de alcohol en niños y adolescentes ha ido en aumento: 7 de cada 10 alumnos de nivel medio han tomado alguna vez en la vida y casi 6 de cada 10 (57,8%) de los mayores de 15 años lo han hecho en el último mes[1]. Por este motivo, desde la Sociedad Argentina de Pediatría (SAP) se pronunciaron sobre este problema, recomendando que los menores de 18 años no consuman alcohol.
“La enzima que metaboliza el alcohol en el hígado funciona correctamente recién entre los 18 y los 20 años, por lo que las borracheras en los adolescentes son más agudas y más dañinas para sus neuronas”, explicó la Dra. Graciela Morales, médica pediatra y Secretaria del Grupo de Trabajo de Adicciones de la SAP.
En la situación actual de nuestro país, en la que la ingesta de bebidas alcohólicas comienza a temprana edad, los padres suelen encontrarse sin respuestas cuando sus hijos se inician en las salidas nocturnas y se exponen al consumo. Por eso, desde la SAP desarrollaron cinco consejos para promover que los chicos crezcan saludablemente, sin que la bebida sea un problema:
- Inculcarle valores desde niño. Por lo general, los padres se preocupan por el alcohol cuando sus hijos entran en la adolescencia, pero la realidad es que diversas actitudes, como la tolerancia a la frustración, el cuidado de las pertenencias y el aprender a compartir son algunas de las cualidades que contribuyen a una juventud saludable. Éstas deben trabajarse desde el nacimiento como parte de una crianza sana, que desembocará en conductas positivas a lo largo de las diversas etapas de la vida.
Al respecto, la Dra. Morales destacó que “en el consultorio, a muchos niños no les gusta que los revisen, entonces lloran; esto es totalmente normal. Los padres, en ocasiones, con la mejor intención, les dan el celular para que no se angustien. Yo les digo que no lo hagan: el niño debe poder expresar lo que no le gusta, es natural. Con el tiempo, aprenderá que es necesario y lo tolerará”.
- Ocupar el rol de adulto responsable. Para que los hijos reconozcan en sus padres un ejemplo a seguir, éstos deben ser medidos en sus acciones. Tomando el caso del alcohol, si bien perfectamente pueden beber en moderada cantidad en una reunión social o con la comida, deben transmitir que éste es un consumo controlado y espaciado. Esto se reproduce en otros ámbitos en los que el adulto funciona como un ejemplo.
- Proponer una relación asimétrica. Los padres no deben intentar ser ‘amigos’ de sus hijos, sino que son quienes deben marcar límites y poner un freno ante actitudes contraproducentes de los adolescentes. Muchos manifiestan que prefieren que sus hijos beban en su casa para que estén contenidos e inclusive les compran el alcohol.
“Si los progenitores están de acuerdo con el consumo, se subvierten los roles y el chico se confunde. Es probable que, a pesar de la negativa, el adolescente consuma igual, pero lo hará sabiendo que está desobedeciendo a sus padres”, comentó la Lic. Adriana Narváez, Psicóloga y Miembro del Grupo de Trabajo en Adicciones de la SAP.
- Generar un vínculo en el que haya diálogo. En relación con el punto anterior, el padre no debe ser ni muy autoritario ni permitir cualquier conducta. Se debe buscar lograr una relación en la que el chico le pueda transmitir sus sentimientos, miedos e inseguridades y en la que los papás le puedan hacer entender que se preocupan por su salud y su bienestar.
- Fomentar su seguridad y madurez. Es importante aceptarlos como son, valorar sus avances y darles responsabilidades para que puedan tomar su propio camino y desarrollarse.
“Los grandes temas a los que los padres les deben prestar atención son los consumos abusivos, la violencia y las relaciones sexuales de riesgo. Todos estos pueden ser abordados a partir del diálogo y con una crianza presente y sana por parte de los cuidadores”, detalló la Dra. Morales, quien además es Especialista en Adolescencia.
La experimentación es característica de la adolescencia, por lo que éste no es el principal obstáculo, sino que debe ponerse el foco en la normalización del consumo. “Hoy, la cultura los impele al exceso, y los fines de semana muchos toman hasta el coma alcohólico, con los riesgos de salud que esto implica. Además, pueden ser víctimas de accidentes de tránsito”, subrayó la Lic. Narváez, quien también es especialista en adolescencia y adicciones.
El modelo islandés
En Islandia, realizaron un abordaje multifacético ante el problema del consumo de alcohol en jóvenes con resultados sorprendentes: En 1998, el 47% de los adolescentes había probado la bebida, mientras que hoy lo ha hecho menos del 5%.
Durante una década, estudiaron los hábitos de consumo de los chicos y encontraron tres elementos sobre los cuales trabajar para reducir la ingesta: retrasar la edad de consumo, idealmente hasta los 18 años; que los jóvenes pasen al menos una hora con su familia y que realicen al menos una actividad extracurricular.
“Para lograr esas tres metas, tomaron diversas medidas, algunas poco populares. Si bien el contexto argentino actual no es el mismo que el de Islandia cuando comenzó el modelo, siempre es interesante conocer casos de éxito para analizar qué se puede replicar en nuestro país”, expresó la Dra. Morales.
Para lograr el primer cometido, la edad legal para comprar bebidas alcohólicas pasó de 18 a 20 y se endurecieron los controles. Por otra parte, se prohibió que los menores de 12 años caminaran solos por la calle después de las 20 horas y que los chicos de entre 13 y 16 años lo hicieran pasadas las 22. Con esto se buscó que pasen más tiempo con sus padres. Por último, desde el Estado becaron y promovieron las actividades extracurriculares para que más niños se inscribieran.
La marihuana
Desde la SAP, también destacaron el aumento en el consumo de marihuana. Lo que les preocupa no es solamente este hecho, sino que el cannabis no cuente con condena social: fumar un ‘porro’ se banaliza y es visto como divertido, dejando de lado las consecuencias graves que puede traer a la salud de los adolescentes. “Suele ocurrir algo similar al alcohol: muchos padres que han experimentado con marihuana en la adolescencia prefieren que sus hijos fumen en su casa e inclusive con ellos, evitando así que consuman en algún lugar peligroso o desconocido”, explicó la Lic. Narváez.
Según los resultados del “Sexto Estudio Nacional sobre consumo de Sustancias Psicoactivas en Estudiantes de Enseñanza Media”[2] realizado por SEDRONAR, la marihuana es la sustancia ilícita de mayor consumo entre los jóvenes escolarizados. El trabajo mostró que casi 1 de cada 10 (8,6%) niños de entre 12 y 17 años consumió marihuana alguna vez en la vida, y el 2,7% lo hizo durante el último mes.
Qué hacer ante una borrachera aguda
En el caso de una emergencia, en la que un adolescente bebió demasiado y se descompuso, desde la SAP recomiendan llevar adelante los siguientes pasos:
- Hablarle. Así, se evita que se quede dormido. Es importante que mantenga el foco de atención.
- Ubicarlo de costado. De esta manera, si el chico vomita, no corre riesgo de ahogarse.
- Abrigarlo. Una de las complicaciones más graves es la hipotermia, por lo que es importante mantener su temperatura corporal.
- No bañarlo. En ocasiones, para despabilarlo, los amigos creen que es una buena idea que se duche. Sin embargo, esto no es recomendable porque también predispone a la hipotermia.
- Llamar a la familia. Si bien se suele pensar que hay que evitar contarles a los padres por miedo a que se enojen, cuando el chico corre peligro, los papás deben enterarse y, lejos de enfadarse, suelen mostrarse preocupados por la salud de su hijo.
- Consulta médica. Si el joven no mejora con las primeras medidas, solicitar asistencia médica inmediata, incluso trasladando al paciente a la guardia médica más cercana.
Alarmante avance del cáncer: 7 cosas que podés hacer para prevenirlo
Un informe difundido este martes por el Centro Internacional de Investigación sobre el Cáncer (IARC) reveló un “alarmante” avance del cáncer en el mundo. En Argentina, se estima que una de cada cinco personas desarrollará la enfermedad.
El organismo dependiente de la Organización Mundial de la Salud aseguró que este año habrá 18 millones de casos nuevos en el mundo, y que morirán casi 10 millones de personas. El cáncer más agresivo sigue siendo el de pulmón (18,4% del total), seguido del colorrectal, estómago e hígado. “Es urgente poner en marcha políticas eficaces de prevención y detección precoz para completar los tratamientos”, reclamó Christopher Wild, director del IARC.
“El cáncer no es una enfermedad única, sino un grupo de enfermedades relacionadas. Muchas cosas en nuestros genes, nuestro estilo de vida y el medio ambiente que nos rodea aumentan o disminuyen el riesgo de presentar cáncer”, advierte en su sitio web el Instituto Nacional del Cáncer de Estados Unidos. Especialistas consultados por Clarín señalan que las estadísticas argentinas no difieren del promedio mundial, y que hay cosas que todos podemos hacer para minimizar algunos de los principales factores de riesgo.
Bajar de peso
En un reciente documento, la Sociedad Argentina de Nutrición (SAN) enumeró 20 razones de salud para bajar de peso. “Debemos tener en cuenta que la obesidad es una enfermedad en sí misma y ello conlleva dejar de lado la culpabilidad de las personas que la padecen, ya que no es un problema de falta de voluntad, sino que es una patología ligada al estilo de vida y su tratamiento es complejo porque vivimos en un ambiente obesogénico que favorece el sobrepeso”, afirmó Mónica Katz, especialista en obesidad y miembro titular de la SAN. Una de esas 20 razones es la relación entre la obesidad y varios tipos de cáncer, de la que se tiene cada vez más evidencia. Estos tumores son los de colon, útero, mama, riñón, ovario, páncreas, próstata, esófago, hígado y algunos tipos de linfoma. “El mantenimiento de un peso corporal normal y una alimentación saludable previenen” el cáncer, dice el documento.
Comer más frutas y verduras
Si bien no existe una “dieta anticáncer”, hay alimentos que tienen un efecto protector y que, además, ayudan a controlar el peso. El Ministerio de Salud recomienda “adoptar una dieta saludable que se caracterice por una baja ingesta de grasas de origen animal (fiambres, embutidos, manteca y leche entera, por ejemplo) y de ácidos grasos trans (presentes en la margarina, los productos de pastelería y las golosinas, entre otros)” y en cambio sugiere consumir más “frutas y verduras (al menos 400 gramos por día), así como legumbres, cereales integrales y frutos secos”.
Dejar de fumar
Está probado que el tabaquismo se vincula directamente con el aumento de riesgo de muchos tipos de cáncer y está probado que es la causa principal, además del cáncer de pulmón, del de vejiga, cuello uterino, esófago, riñón, cavidad oral, páncreas, estómago y la leucemia mielógena aguda. “No fumar o dejar de fumar disminuye el riesgo de cáncer y de morir por esta enfermedad. Los científicos consideran que el consumo de cigarrillos provoca casi 30 % de todas las muertes por cáncer en los Estados Unidos”, advierte el Instituto Nacional del Cáncer de Estados Unidos (NCI).
Moderar el consumo de alcohol
El consumo abusivo de bebidas alcohólica puede estar relacionados con riesgo más alto de cáncer de esófago, cavidad oral, colorrectal, mama e hígado. Según la Asociación Americana de Oncología Clínica (ASCO), esto puede deberse a dos químicos, el etanol (la parte principal de las bebidas) y el acetaldehído (que se fabrica cuando es digerido en el cuerpo), que pueden dañar el ADN de las células saludables. El alcohol también puede afectar la descomposición de la hormona estrógeno, que aumenta su cantidad en sangre: tener más estrógeno en el cuerpo que lo habitual es un factor de riesgo para los cánceres de mama, de ovarios y de útero. Además, se estima que puede debilitar la capacidad del cuerpo de procesar y absorber algunas vitaminas y minerales, y causar aumento de peso. ASCO sugiere limitar la cantidad de bebidas alcohólicas a una por día para las mujeres, y a entre una y dos para los hombres. Se considera una bebida a 341 ml de cerveza, 142 ml de vino o 43 ml de un licor con 80 de graduación alcohólica.
Hacer actividad física
Otro estudio reciente difundido por la OMS muestra que en el mundo una de cada tres mujeres y uno de cada cuatro hombres no tienen una actividad física suficiente para gozar de buena salud. La actividad física no sólo reduce el riesgo de cáncer, sino también de otras enfermedades crónicas, como las cardíacas y la diabetes. “Existen muchas investigaciones en curso sobre la actividad física y sus efectos en el cáncer. Las investigaciones recientes muestran que incluso la actividad leve puede brindar algunos beneficios para la salud. La actividad leve incluye todo lo que haga para evitar estar sentado o acostado”, dice la ASCO.
Entre otros, se probó que hacer actividad física regular disminuye el riesgo de sufrir cáncer de colon, de útero, de pulmón y de mama. Sobre este último, dicen que “algunos estudios muestran que mientras más elevado sea el nivel de actividad, menor es el riesgo de cáncer. Sin embargo, no se sabe con certeza si se debe alcanzar algún nivel de actividad específico para reducir el riesgo. Si bien la actividad durante toda la vida de una persona es importante, a cualquier edad puede ayudar a reducir el riesgo de cáncer de mama”. Y sigue: "La actividad física de moderada a enérgica es la que lo hace sudar y que hace que su corazón lata más rápido. Incluye caminar, nadar, andar en bicicleta o correr. Una cantidad cada vez más amplia de investigaciones sugiere que hacer cualquier tipo de actividad para evitar estar sentado durante mucho tiempo ayuda a reducir el riesgo de cáncer".
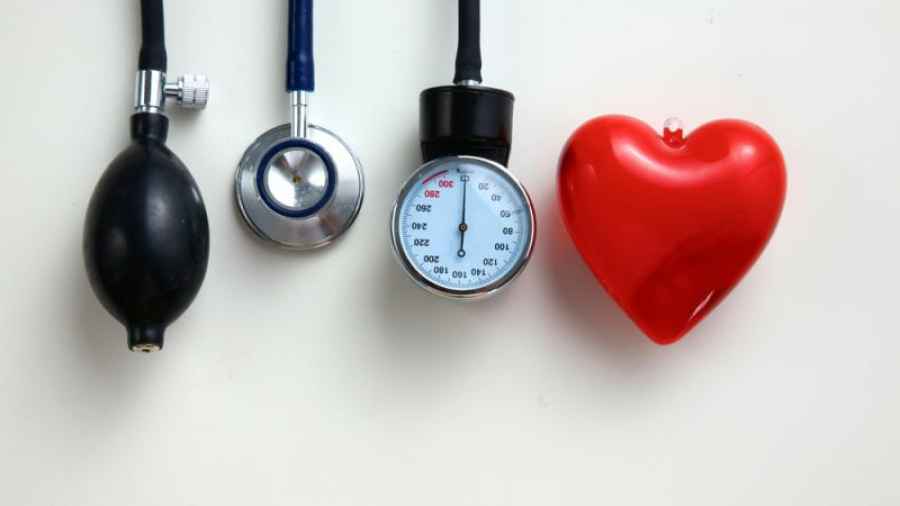
Cumplir con los controles
La detección precoz es clave para tener un buen pronóstico en el tratamiento de la enfermedad. Por eso es importante la consulta de rutina con el médico clínico y los chequeos específicos, como la mamografía para las mujeres, los controles de próstata para los hombres y las colonoscopías a partir de los 45 años. “En los estadios iniciales, el cáncer de mama no produce síntomas. Por eso, la mamografía, la ecografía y, en ciertos casos, la resonancia magnética son fundamentales para detectar lo que aún no se puede tocar”, dice Luciano Cassab, miembro de la Sociedad Argentina de Mastología. La videocolonoscopía, que se hace con sedación, es importante porque la patología neoplásica del colon ocupa el segundo lugar en el hombre y el tercero en la mujer dentro de las enfermedades malignas en Argentina, con una mayor incidencia después de los 50 años e igual prevalencia en ambos sexos.
Si bien en el cáncer las cuestiones genéticas y hereditarias son grandes, existen tests que en algunos casos, bajo indicación médica, pueden ayudar con los diagnósticos tempranos.
Protegerse del sol
El melanoma es el cáncer más frecuente, aunque su mortalidad es menor comparada con otras patologías. Es importante protegerse adecuadamente de los rayos ultravioleta: evitar el sol en los horarios “prohibidos”, utilizar protector solar de un factor adecuado antes de exponerse, usar sombreros y lentes, y nunca tomar cama solar. También, controlar periódicamente los lunares con un dermatólogo.
Fuente: Clarín salud
Larvas de moscas elaboran una sustancia que puede curar heridas crónicas
Una herida común cicatriza en un lapso de tiempo relativamente corto. El proceso de cicatrización comprende tres etapas: inflamación, proliferación y regeneración. Las heridas crónicas son aquellas que permanecen en estado inflamatorio y no cicatrizan al cabo de seis meses. Tal es el caso de las úlceras que la leishmaniasis provoca. O el de las heridas de pie diabético, que suelen derivar en amputaciones.
Una forma antigua de tratamiento, que se había dejado de lado con el surgimiento de los antibióticos, está siendo rehabilitada ahora en algunos hospitales de Estados Unidos, Europa y Latinoamérica. En Brasil, se la aplica en el Hospital Universitario Onofre Lopes de la ciudad de Natal, capital del estado de Rio Grande do Norte.
Se trata de la terapia larval o larvoterapia, que consiste en la utilización de larvas de moscas para remover tejidos necrosados, romper la biopelícula bacteriana, eliminar bacterias, y promover el crecimiento de tejido sano. Más allá de su carácter aparentemente repulsivo, este tratamiento se ha mostrado bastante eficiente en la cura de esas heridas persistentes.
Este tema constituye el objeto de estudio de Andrea Díaz Roa, doctoranda en el Laboratorio Especial de Toxinología Aplicada del Centro de Toxinas, Respuesta Inmunitaria y Señalización Celular (CeTICS), un Centro de Investigación, Innovación y Difusión (CEPID) financiado por la Fundación de Apoyo a la Investigación Científica del Estado de São Paulo (FAPESP). Nacida en Colombia y posgraduanda en Ciencias Biomédicas en la Universidad del Rosario, de Bogotá, Díaz Roa es dirigida en el CeTICS por Pedro Ismael da Silva Jr., investigador científico del Instituto Butantan, en São Paulo.
“Ella realizó un trabajo pionero y realmente innovador sobre el péptido antibacteriano sarconesina, producido por la larva de la mosca Sarconesiopsis magellanica”, declaró Da Silva Jr. a Agência FAPESP. Este trabajo se dio a conocer durante la 47ª Reunión Anual de la Sociedad Brasileña de Bioquímica y Biología Molecular, realizada en mayo en la localidad de Joinville (en el estado de Santa Catarina).
Díaz Roa fue la primera en identificar, secuenciar y describir la estructura de ese péptido al que le dio el nombre de sarconesina, en una referencia a la mosca Sarconesiopsis. La idea es utilizar esta sustancia como principio activo en la elaboración de un medicamento. Por ser una molécula relativamente pequeña, la sarconesina puede sintetizarse en laboratorio de manera totalmente artificial. O puede elaborársela mediante ingeniería genética, a través de la introducción de las bases de ADN que la codifican en una bacteria huésped.
“Conocemos su secuencia de aminoácidos, hemos evaluado su actividad antimicrobiana con relación a diversos tipos de bacterias y estamos pensando en efectuar una solicitud de patente”, dijo Da Silva Jr.
Normalmente, los péptidos antimicrobianos actúan rompiendo las membranas de los microorganismos adversarios. Esta acción es puramente electrostática. Las membranas son eléctricamente negativas y los péptidos son eléctricamente positivos. Al atraerse, los péptidos se adhieren a las membranas y les sustraen fragmentos. Los contenidos de los microorganismos se escurren a través de los orificios y las bacterias terminan muriéndose.
“Pero no es esto lo que sucede con la sarconesina. Sabemos que ésta es eléctricamente neutra. Nuestra hipótesis indica que, de alguna manera, los microorganismos la incorporan y el péptido actúa en ellos desde el interior, desestructurando el ADN o el ARN. Aún estamos investigando este mecanismo”, explicó Da Silva Jr.
Díaz Roa comenta que está abordando este tema de dos maneras. Por un lado, transformando la sarconesina en medicamento, sin terapia larval. Por el otro, implementando la práctica de la larvoterapia en Brasil.
Recientemente, la científica estuvo en Estados Unidos visitando el laboratorio de Ronald Sherman, considerado “el padre de la larvoterapia moderna”. El proyecto de Díaz Roa apunta ahora a radicarse en Brasil y empezar a aplicar este procedimiento médico en el país.
“Las moscas se crían en laboratorio y ponen sus huevos sobre material orgánico. Luego se disponen las larvas estériles en el interior de las heridas, donde permanecen entre 24 y 48 horas. En promedio se emplean 20 larvas por centímetro cuadrado. Las heridas quedan cubiertas durante el procedimiento y se las lava tras el retiro de las larvas. Dependiendo del caso, una sola aplicación es suficiente. Las larvas se alimentan únicamente de la parte necrosada de las heridas”, dijo Díaz Roa.
Dejando de lado la repugnancia que la larvoterapia puede provocar, este procedimiento en sí mismo no es más molesto que las propias heridas. Éstas generalmente pican, duelen o exudan.
En los casos de úlceras de pie diabético, la desensibilización que provoca la propia enfermedad impide que los pacientes sientan molestias. Y la terapia larval por sí sola puede promover la reversión total del cuadro.
Con relación a la leishmaniasis cutánea, su acción es únicamente coadyuvante, pues la persistencia de la herida es el resultado de la presencia activa del protozoo del género Leishmania, que inflama la zona. El tratamiento principal en este caso consiste en matar al parásito con medicamentos bastante tóxicos controlados por las agencias de salud. Y el papel de la larvoterapia será el de promover la cicatrización de la herida, cosa que suele tardar bastante tiempo en ocurrir. (Fuente: AGÊNCIA FAPESP/DICYT)
Fuente: COFA
Lo más visto
- Covishield, la vacuna que India lanzó con Oxford-AstraZeneca
- El gobierno establece los requisitos para la producción de cannabis medicinal
- Anmat aprobó en el país la primera vacuna que protege contra el dengue
- Comunicación de Novo Nordisk: Diferencias en la indicación de Victoza® y Saxenda®
- Ibupirac declarado apto para celíacos