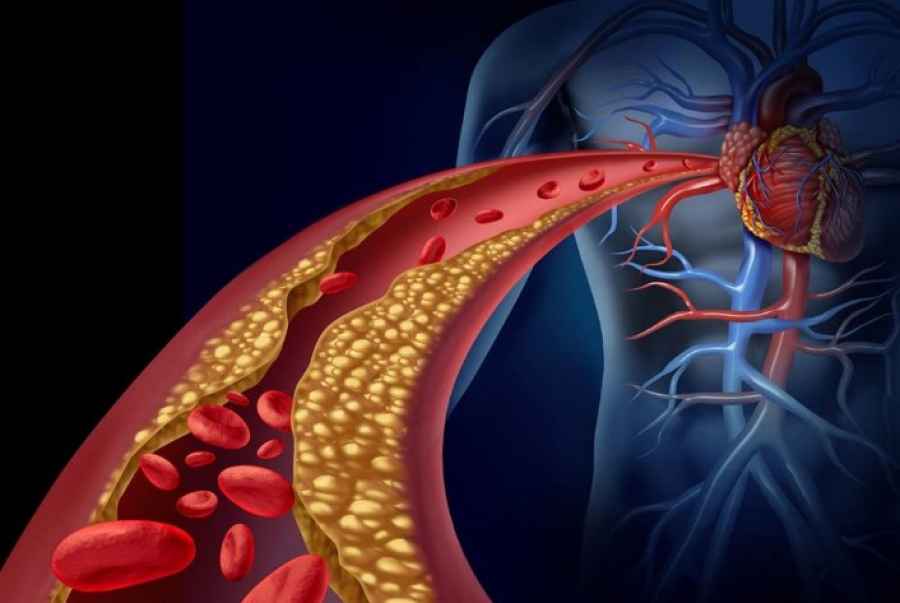
Descubren cómo el LDL entra en las paredes de las arterias
Investigadores de la UT Southwestern (Estados Unidos) han determinado cómo el LDL, conocido como ‘colesterol malo’, entra en las paredes de las arterias para causar la placa que estrecha los vasos sanguíneos y conduce a ataques cardíacos y accidentes cerebrovasculares.
El estudio, publicado en la revista ‘Nature’, revela por primera vez cómo una proteína llamada SR-B1 transporta partículas de LDL hacia y luego a través de las células endoteliales que recubren las arterias. Además, los investigadores también encontraron una segunda proteína denominada DOCK4 que se asocia con SR-B1 y es necesaria para este proceso.
En las primeras etapas de la aterosclerosis, el LDL que ha entrado en la pared arterial atrae y es engullido por importantes células del sistema inmunológico llamadas macrófagos que ‘comen’ partículas de LDL. Los macrófagos cargados de LDL se convierten en células que promueven la inflamación y el desarrollo de placas ateroscleróticas.
Las placas estrechan las arterias y pueden volverse inestables. Las placas que se rompen pueden activar la coagulación de la sangre y bloquear el flujo sanguíneo al cerebro o al corazón, lo que resulta en un accidente cerebrovascular o un ataque cardíaco. En estudios de ratones con colesterol elevado, los investigadores determinaron que la eliminación de la SR-B1 de las células endoteliales que recubren los vasos sanguíneos resultó en mucho menos LDL entrando a la pared arterial, menos células de espuma formadas y placas ateroscleróticas que eran considerablemente más pequeñas.
“Al comienzo de este trabajo era sorprendentemente desconocido cómo el LDL entra en la pared arterial para causar enfermedad cardiovascular. Los hallazgos del documento resuelven ese misterio y contrarrestan la suposición previa de muchos científicos de que el LDL simplemente entra a través de sitios de daño o disrupción en la capa única de células endoteliales que sirve como barrera protectora de la pared de la arteria”, explica el autor principal del trabajo, Philip Shaul.
Fuente: Europa Press / COFA
La FDA aprueba el primer tratamiento para pacientes pediátricos con lupus
La FDA aprobó belimumab (Benlysta – GlaxoSmithKline) I.V. Infusión para el tratamiento de niños con lupus eritematoso sistémico (LES). Belimumab ha sido aprobado para su uso en pacientes adultos desde 2011; sin embargo, esta es la primera vez que la FDA aprueba un tratamiento para pacientes pediátricos con LES. “La agencia aceleró la revisión y aprobación de esta solicitud porque Benlysta I.V. satisface una necesidad de terapias, específicamente en pacientes pediátricos con LES”, dijo Janet Woodcock, MD, directora del Centro para la Evaluación e Investigación de Medicamentos de la FDA. “Si bien no existe una cura para el lupus, el tratamiento puede ayudar a nuestros pacientes más jóvenes a controlar su enfermedad con la esperanza de mejorar su calidad de vida y reducir el riesgo de daño orgánico y discapacidad a largo plazo”.
La información de seguridad para profesionales de la salud y pacientes incluye una advertencia de mortalidad, infecciones graves, hipersensibilidad y depresión, basada en los datos de los estudios clínicos en adultos con LES. Además, no se debe administrar belimumab con vacunas vivas, y GlaxoSmithKline debe proporcionar una guía para informar a los pacientes sobre los riesgos asociados con el medicamento.
Los efectos adversos más comunes en los pacientes incluyeron náuseas, diarrea y fiebre. Debido a que las reacciones a la infusión también fueron comunes, se incluye una recomendación a los profesionales de la salud de que traten previamente a los pacientes con un antihistamínico.
Fuente: Pharmacy Times / COFA
Migraña: la sufren uno de cada 10 argentinos y llega al país la primera droga específica para tratarla
Un dolor de cabeza intenso, pulsátil, generalmente de un solo lado. Náuseas, vómitos y sensibilidad extrema a la luz o al ruido. Un malestar que hace insoportable las actividades cotidianas para quienes lo padecen. Que son, en Argentina, una de cada 10 personas. Eso detectó el primer estudio de prevalencia de migraña en el país, realizado por la consultora Poliarquía con especialistas de la Sociedad Neurológica Argentina, en el marco del lanzamiento del primer medicamento específico para tratar la enfermedad.
Encuestaron a 2.500 personas, a quienes les aplicaron un cuestionario específico de migraña validado internacionalmente (el Migraine Screen Questionnaire, MSQ), con el objetivo de comprender el alcance y las características de la enfermedad. ¿Los principales resultados? El 53% de los encuestados sufrió al menos un dolor de cabeza en los últimos 12 meses y el 9,5% respondió afirmativamente a las preguntas que determinan que ese dolor es migraña.
Respecto del motivo que dispara los dolores de cabeza, de manera contundente el 40% de los migrañosos afirma que el episodio de migraña está desencadenado por el estrés emocional. En menor medida lo asocian con dificultades o la modificación de su sueño habitual (11%) y un 10% menciona la relación de los dolores de cabeza con la menstruación o cambios hormonales.
"Muchas de las personas que sufren de los síntomas de la migraña desconocen que es una enfermedad neurológica, que tiene tratamiento y es controlable. Nuestra responsabilidad como especialistas en Neurología, y de la sociedad en general, es informar, educar y lograr que aquellos para quienes el dolor de cabeza es un problema en su vida consulten a un médico. Sólo de esa manera podremos ayudar a los pacientes a cambiar su calidad de vida a través de un tratamiento efectivo”, resume la doctora María Teresa Goicochea, neuróloga de Clínica del Dolor de Fleni.
La Administración Nacional de Medicamentos y Tecnología Médica (ANMAT) acaba de aprobar en el país un fármaco que promete ser un cambio de paradigma en el tratamiento de la enfermedad. El erenumab es el primero específico para la migraña y ya se vende desde hace un año en Estados Unidos. Se inyecta cada mes con un aparato como el de la insulina y logra reducir tanto la intensidad como la frecuencia de los ataques. La droga bloquea un fragmento proteico conocido como CGRP, que provoca y prolonga las migrañas. Si bien aún no se informó el valor que tendrá el tratamiento en Argentina, en Estados Unidos cuesta unos 7.000 dólares anuales.
El porcentaje de los migrañosos que consultó alguna vez a un médico es bastante alto (un 62%), pero sólo el 37% vio a un especialista en neurología o dolor. Y 6 de cada 10 se automedican con analgésicos para combatir el dolor, al que más de la mitad califica como severo y un 30%, como moderado. Y la mitad de quienes sufren migraña conceden que la enfermedad afecta sus actividades físicas e intelectuales. Casi todos ellos (el 94%) tienen problemas para dormir y más de la mitad (56%) tuvo que faltar al trabajo por la crisis de dolor. Además, la mitad de los migrañosos sienten que los demásno comprenden el malestar por el que atraviesan.
“La migraña permanece con bajos niveles de reconocimiento y tratamiento. Existen en Argentina muchas personas sin diagnosticar que recurren a la automedicación, lo cual provoca efectos rebote que complejizan aún más el cuadro. Es por eso que a quienes sufren fuertes dolores de cabeza los especialistas recomendamos consultar al médico, obtener su diagnóstico y comenzar un tratamiento efectivo que permita mejorar su calidad de vida y recuperar el tiempo perdido causado por esta enfermedad impredecible”, asegura Daniel Doctorovich, Médico Neurólogo, jefe de la Sección Cefaleas del Hospital Italiano.
La migraña es tres veces más común en mujeres que en hombres y afecta con mayor frecuencia a personas de entre 15 y 50 años. ¿Qué es lo que la provoca? “No es algo que se adopta. La migraña es causada por una predisposición genética cerebral a reaccionar de más a algunos estímulos. Por eso resulta imprescindible hablar de ella y visibilizarla, para que la sociedad en su conjunto comprenda que no es sólo un simple dolor de cabeza sino que es una enfermedad que sin un adecuado tratamiento reduce la posibilidad de llevar una vida normal”, concluye Fiorella Martín Bertuzzi, también del Servicio de Neurología del Italiano.
Fuente: Clarín Salud
Día Mundial de la Hipertensión Pulmonar en Rosario
La Hipertensión Pulmonar se define por el desmesurado aumento de la presión en las arterias que llevan la sangre del corazón y a los pulmones causando falta de aire (disnea), cansancio (fatiga), mareos, tos seca, síncopes (pérdida de conocimiento) y otros síntomas. Éstos se exacerban con el ejercicio -por ejemplo al subir escaleras- y que de no diagnosticarse y recibir tratamiento en forma precoz, lleva inevitablemente al fallo cardíaco. Suele confundírsela con asma o ataques de pánico. Estadísticamente, la padecen 52 personas por cada millón, esto significa que 25 millones de personas presentan Hipertensión Pulmonar en el mundo. Es más frecuente en el sexo femenino y la edad de mayor presentación oscila entre los 20 y 50 años. En Argentina hay aproximadamente 2.500 pacientes con ésta enfermedad, y muchos de ellos atraviesan sucesivas consultas con distintos profesionales hasta alcanzar el diagnóstico correcto. Su detección a tiempo es esencial para que los pacientes puedan tener una mayor expectativa y una mejor calidad de vida.
Las actividades en la ciudad de Rosario, comenzarán en el Boulevard Oroño y Córdoba, donde la asociación civil HIPUA (Hipertensión Pulmonar Argentina) repartirá a partir de las 9:00hs folletos informativos, destinados a la difusión y concientización acerca de la existencia de la HP y los síntomas que la caracterizan.A 10:00hs, en la Fundación Dr. Villavicencio, se ha previsto realizar varias charlas a la comunidad, pacientes y familiares.Se expondrá acerca del rol de una asociación de pacientes para difundir, orientar, concientizar y contener a todas aquellas personas que padecen HP. El Dr. Cristian Botta, coordinador del grupo de Insuficiencia Cardíaca e Hipertensión Pulmonar del Hospital Cullen de Santa Fe, presentará su charla sobre “Diagnostico y Tratamiento del HP”.Debido a la importancia del ejercicio físico en personas que portan la enfermedad, se enseñarán distintas técnicas de fácil aplicación.Seguidamente se llevará a cabo una caminata simbólica de pacientes y sus familias, los que serán continuamente monitoreados y controlados por personal de salud allí presente.
En simultáneo en la sede del Grupo Oroño,el equipo médico de la institución, bajo la coordinación de los Dres. Fabián Diez, Ana Diez y Juan Pablo Escalante junto a especialistas en Cardiología, Neumonología y Reumatología realizarán la evaluación Integral de personas con sospecha clínica de Hipertensión Pulmonar. También a aquellos pacientes portadores sin seguimiento, para lograr un mejor pronóstico a largo plazo, los que serán sometidos a exámenes como ECG, espirometría, capiloroscopía, ecocardiograma doppler, test de caminata, entre otros.
HIPUA, desde el año 2009, es la única asociación en la Argentina integrada por pacientes, familiares y amigos que colaboran y prestan su tiempo de manera desinteresada. Su misión es brindar información, asesoramiento y contención a todas aquellas personas (niños, adolescentes y adultos) que han recibido el diagnóstico de Hipertensión Pulmonar y asistirlos para mejorar su calidad de vida. Sus actividades han sido declaradas de Interés Sanitario por la Cámara del Senado de la Nación y la Legislatura del Gobierno de la Ciudad Autónoma de Buenos Aires.
Con estas acciones, el Grupo Oroño como organizador y promotor de la realización de esta Jornada junto a HIPUA, esperan avanzar en el mejoramiento del acceso a la asistencia médica, aumentar la concientización y detección temprana de la HP, fomentar la investigación clínica y la innovación, y ayudar a los pacientes y sus familias.
VGLL3, la molécula que hace que las mujeres sean más propensas a contraer lupus
Un equipo de investigadores de la Universidad de Michigan (UM) en EE.UU demostró, a través de un estudio en ratones, que las mujeres sufren más enfermedades autoinmunes, como el lupus, por la elevada presencia molecular de VGLL3 en la piel.
El estudio, publicado en ‘JCI Insight’, ha tratado de explicar cómo la VGLL3 supone el desarrollo de diferentes trastornos y eventos en la piel que activan el sistema inmunitario, aún cuando no hay nada contra lo que defenderse. En esta investigación, los expertos explicaron que la elevada presencia de esta molécula en las células que conforman la piel pone en funcionamiento el sistema inmunológico, el cual produce una respuesta inmune autoatacante que afecta tanto a la dermis como a los órganos internos.
En el estudio se pudo ver que las hembras de ratones tenían una presencia de VGLL3 en la piel más alta que los ratones machos.
En este sentido, los investigadores señalaron que la elevada presencia de esta molécula en la piel modifica los niveles de expresión de genes que conforman el sistema inmunológico. Así, han observado que estos cambios hacían que la piel de los ratones se volviese escamosa. Esto ocurre porque las células inmunitarias se incrementan, inundando la piel y los ganglios linfáticos, lo que conlleva la aparición de anticuerpos que pueden afectar a órganos internos.
Fuente: Europa Press / COFA
Comunicado: uso responsable del ibuprofeno
A partir de la información emitida por la Agencia Nacional de Seguridad de Medicamentos de Francia (ANSM) que advierte sobre la relación entre el consumo de Ibuprofeno y un posible riesgo de agravamiento de infecciones, y teniendo en cuenta el comunicado de la ANMAT, que informó que “continúa analizando, en consulta con las sociedades científicas, el ingrediente activo con el objeto de realizar una evaluación constante del mismo”, la Confederación Farmacéutica Argentina recomienda a las personas que toman este medicamento en sus diversas presentaciones, que realicen un uso responsable del mismo.
En su presentación de venta bajo receta, se debe respetar las indicaciones del médico en cuanto a dosificación e intervalo de toma. Y en la presentación de venta libre debe tomarse por un periodo de 3 a 5 días, respetando la dosificación indicada en el prospecto.
- No se debe tomar por un periodo mayor sin consultar al médico.
- No se debe aumentar la dosis en caso de no lograr el efecto deseado, sino consultar al médico.
- Todos los medicamentos se deben adquirir en las farmacias para tener garantía de su origen, calidad y conservación.
- Ante cualquier duda, consultar al médico y/o al farmacéutico.
En la Argentina el ibuprofeno es uno de los productos más vendidos. Se consumieron en 2018 un total de 27.679.801 unidades de este producto (sin asociaciones).
En investigación: Empagliflozina podría revertir la insuficiencia cardíaca
Investigadores de la Escuela de Medicina Icahn en Mount Sinai (Estados Unidos) demostraron que la empagliflozina, un fármaco antidiabético, puede tratar y revertir la progresión de la insuficiencia cardiaca en modelos animales no diabéticos, y lograr que el corazón produzca más energía y funcione de manera más eficiente.
“Este medicamento podría ser un tratamiento prometedor para la insuficiencia cardiaca en pacientes no diabéticos y diabéticos. Nuestra investigación puede llevar a una aplicación potencial en humanos, salvar vidas y mejorar la calidad de vida”, dijeron los investigadores, cuyo trabajo ha sido publicado en el ‘Journal of American College of Cardiology’.
La empagliflozina fue aprobada por la Agencia Americana del Medicamento (FDA, por sus siglas en inglés) en el año 2014, siendo el primer medicamento en la historia de la diabetes tipo 2 que ha demostrado prolongar la supervivencia.
Si bien los pacientes con diabetes suelen tener un mayor riesgo de insuficiencia cardiaca, estudios anteriores han sugerido que aquellos que toman empagliflozina no suelen desarrollar insuficiencia cardiaca. Esas observaciones llevaron a estos científicos a cuestionar si el medicamento contiene un mecanismo, independiente de la actividad antidiabética, que está relacionado con la prevención de la insuficiencia cardiaca, y si podría tener el mismo impacto en los no diabéticos.
Los investigadores probaron la hipótesis induciendo insuficiencia cardiaca en 14 cerdos no diabéticos. Durante dos meses, trataron a la mitad de los animales con empagliflozina y al otro grupo con un placebo. El equipo evaluó los cerdos con resonancia magnética cardiaca, ecocardiografía 3D y cateterización invasiva en tres puntos diferentes del estudio (antes de la inducción, un día después de la inducción y al cabo de dos meses).
A los dos meses, todos los animales del grupo tratados con empagliflozina experimentaron una mejor función cardiaca. Específicamente, esos cerdos tenían menos acumulación de agua en los pulmones (menos congestión pulmonar, que es responsable de causar dificultad para respirar) y niveles más bajos de biomarcadores de insuficiencia cardiaca. Es importante destacar que los ventrículos izquierdos tenían contracciones más fuertes (función sistólica mejorada).
“Este estudio confirmó nuestra hipótesis de que la empagliflozina es un tratamiento eficaz para la insuficiencia cardiaca y no solo un fármaco antidiabético. Además, demostró que la empagliflozina es útil para la insuficiencia cardiaca independientemente del estado diabético de un paciente”, destacaron los autores del estudio.
Fuente: Europa Press / COFA
En investigación: Empagliflozina podría revertir la insuficiencia cardíaca
Investigadores de la Escuela de Medicina Icahn en Mount Sinai (Estados Unidos) demostraron que la empagliflozina, un fármaco antidiabético, puede tratar y revertir la progresión de la insuficiencia cardiaca en modelos animales no diabéticos, y lograr que el corazón produzca más energía y funcione de manera más eficiente.
“Este medicamento podría ser un tratamiento prometedor para la insuficiencia cardiaca en pacientes no diabéticos y diabéticos. Nuestra investigación puede llevar a una aplicación potencial en humanos, salvar vidas y mejorar la calidad de vida”, dijeron los investigadores, cuyo trabajo ha sido publicado en el ‘Journal of American College of Cardiology’.
La empagliflozina fue aprobada por la Agencia Americana del Medicamento (FDA, por sus siglas en inglés) en el año 2014, siendo el primer medicamento en la historia de la diabetes tipo 2 que ha demostrado prolongar la supervivencia.
Si bien los pacientes con diabetes suelen tener un mayor riesgo de insuficiencia cardiaca, estudios anteriores han sugerido que aquellos que toman empagliflozina no suelen desarrollar insuficiencia cardiaca. Esas observaciones llevaron a estos científicos a cuestionar si el medicamento contiene un mecanismo, independiente de la actividad antidiabética, que está relacionado con la prevención de la insuficiencia cardiaca, y si podría tener el mismo impacto en los no diabéticos.
Los investigadores probaron la hipótesis induciendo insuficiencia cardiaca en 14 cerdos no diabéticos. Durante dos meses, trataron a la mitad de los animales con empagliflozina y al otro grupo con un placebo. El equipo evaluó los cerdos con resonancia magnética cardiaca, ecocardiografía 3D y cateterización invasiva en tres puntos diferentes del estudio (antes de la inducción, un día después de la inducción y al cabo de dos meses).
A los dos meses, todos los animales del grupo tratados con empagliflozina experimentaron una mejor función cardiaca. Específicamente, esos cerdos tenían menos acumulación de agua en los pulmones (menos congestión pulmonar, que es responsable de causar dificultad para respirar) y niveles más bajos de biomarcadores de insuficiencia cardiaca. Es importante destacar que los ventrículos izquierdos tenían contracciones más fuertes (función sistólica mejorada).
“Este estudio confirmó nuestra hipótesis de que la empagliflozina es un tratamiento eficaz para la insuficiencia cardiaca y no solo un fármaco antidiabético. Además, demostró que la empagliflozina es útil para la insuficiencia cardiaca independientemente del estado diabético de un paciente”, destacaron los autores del estudio.
Fuente: Europa Press / COFA
En investigación: Avanza una vacuna antineumocócica de 20 serotipos
La FDA otorgó en septiembre de 2018 la designación “Breakthrough Therapy” a una vacuna conjugada antineumocócica 20-Valente (20vPnC) en desarrollo en Pfizer. Su indicación propuesta es la prevención de la enfermedad invasiva y la neumonía causada por 20 serotipos de S. pneumoniae en adultos mayores de 18 años. La evidencia clínica preliminar sugirió que esta vacuna podría tener ventajas sustanciales sobre las vacunas disponibles. En 2017, la FDA también otorgó el estado de vía rápida para una indicación pediátrica para 20vPnC.
S. pneumoniae es una causa primaria de neumonía y meningitis adquirida en la comunidad en niños y ancianos.
Las vacunas ahora se administran de manera rutinaria a los niños, y también están disponibles para los adultos. Sin embargo, solo cubren un número de aproximadamente 91 cepas de esta bacteria. A medida que disminuye la infección por 1 cepa, otras cepas a menudo cambian bajo la presión de la inmunización y se vuelven más comunes o virulentas.
En el 29º Congreso Europeo de Microbiología Clínica y Enfermedades Infecciosas (ECCMID) en Ámsterdam, Países Bajos, investigadores actualizaron a los asistentes con hallazgos recientes sobre esta vacuna, actualmente designada por el nombre de laboratorio PF-06482077.
Esta vacuna en ensayo, aumenta los 13 serotipos contenidos en la vacuna antineumocócica conjugada de 13 valencias de Pfizer (Prevnar 13) con 7 serotipos adicionales (8, 10A, 11A, 12F, 15B, 22F y 33F).
El estudio presentado en Ámsterdam fue un ensayo doble ciego, aleatorizado, activo-controlado de fase 2 (N = 444). Todos los participantes tenían entre 60 y 64 años. Recibieron PF-06482077 seguido de placebo al mes, o la vacuna antineumocócica conjugada de 13 valencias, seguida de la vacuna de polivalente polisacárido de 23 valente a 1 mes.
La inmunidad contra el neumococo está mediada por la fagocitosis en presencia de complemento y anticuerpos contra los polisacáridos capsulares neumocócicos. In vitro, las actividades opsonofagocíticas de los anticuerpos séricos imitan las actividades funcionales de los anticuerpos in vivo. Los investigadores usan la actividad opsonofagocítica para predecir la inmunidad protectora.
En este estudio, los investigadores observaron respuestas robustas para los 20 serotipos de vacunas en el grupo 20vPnC. Utilizando la actividad opsonofagocítica como medida, observaron incrementos de la media geométrica desde la línea de base de 6.1 hasta 68.6 para los serotipos en común con la vacuna neumocócica 13-valente conjugada, y de 9 a 112.2 para los 7 serotipos adicionales no incluidos en esa vacuna.
Los eventos adversos se ajustaron a lo que se esperaba de las inmunizaciones, principalmente reacciones leves en el lugar de la inyección (enrojecimiento, hinchazón, dolor).
Los 20 serotipos incluidos en 20vPnC son responsables de la mayoría de las enfermedades neumocócicas circulantes en adultos. Como se señaló, la infección con estos serotipos a menudo conduce a enfermedades graves. Muchos de estos serotipos también están asociados con la resistencia a los antibióticos. En comparación con la enfermedad invasiva, la enfermedad no invasiva (infección del oído medio, sinusitis o bronquitis recurrente) suele ser menos grave, pero mucho más frecuente.
20vPnC entró en la fase 3 de ensayos clínicos en diciembre de 2018.
Fuente: COFA
La EMA y la agencia española advierten sobre quinolonas y fluoroquinolonas de uso sistémico
Se han notificado casos de reacciones adversas incapacitantes, de duración prolongada y potencialmente irreversibles que afectan principalmente a los sistemas musculoesquelético y nervioso, con los antibióticos del grupo de las quinolonas y fluoroquinolonas.
• Por este motivo, para todos los antibióticos pertenecientes a estos grupos farmacológicos, se ha revisado el balance beneficios-riesgo en sus indicaciones autorizadas en el conjunto de la Unión Europea (UE).
• Los medicamentos que contienen cinoxacina, flumequina y ácido nalidíxico (en España no existen medicamentos comercializados con ninguno de estos principios activos), así como ácido pipemídico, se retirarán del mercado.
• Estos medicamentos no deben prescribirse: o para el tratamiento de infecciones autolimitadas o leves (como faringitis, amigdalitis y bronquitis aguda) o para la profilaxis de la diarrea del viajero o de las infecciones recurrentes de las vías urinarias bajas o para infecciones no bacterianas, por ejemplo, prostatitis no bacteriana (crónica) o para infecciones de leves a moderadas (incluidas cistitis no complicadas, exacerbaciones agudas de la bronquitis crónica y la enfermedad pulmonar obstructiva crónica (EPOC), rinosinusitis bacteriana aguda y otitis media aguda), a menos que otros antibióticos comúnmente recomendados para estas infecciones se consideren inadecuados o a pacientes con antecedentes de reacciones adversas graves tras la administración de este tipo de antibióticos
• Estos medicamentos deberán prescribirse con especial precaución a personas de edad avanzada, pacientes con insuficiencia renal, pacientes que hayan recibido trasplantes de órganos sólidos y pacientes tratados concomitantemente con corticosteroides, ya que en estos grupos, el riesgo de sufrir tendinitis y rotura tendinosa puede verse aumentado. Se debe evitar el uso concomitante de corticosteroides con fluoroquinolonas.
• Indique a los pacientes que interrumpan el tratamiento y acudan al médico ante la aparición de los primeros signos/síntomas sugestivos de una reacción adversa grave, como por ejemplo: tendinitis, rotura tendinosa, mialgia, debilidad muscular, dolor y/o tumefacción articular, neuropatía periférica y efectos sobre el sistema nervioso central. Información sobre este asunto de seguridad Se ha revisado la información disponible sobre los antibióticos pertenecientes al grupo de las quinolonas y fluoroquinolonas de uso sistémico e inhalado (estas últimas no comercializadas en España) para evaluar el riesgo de reacciones adversas graves incapacitantes, de duración prolongada (de meses o años de duración) y potencialmente irreversibles, que afectan principalmente a los sistemas musculoesquelético y nervioso. Entre las reacciones adversas graves del sistema musculoesquelético se encuentran: tendinitis, rotura de tendones, mialgia, debilidad muscular, artralgia, tumefacción articular y dificultad al caminar. Entre las reacciones adversas graves sobre el sistema nervioso central y periférico se encuentran: neuropatía periférica, insomnio, depresión, fatiga y alteración de la memoria, así como deterioro de la vista, la audición, el olfato y el gusto. Solo se han notificado unos pocos casos de estas reacciones adversas incapacitantes y potencialmente irreversibles, pero puede asumirse que existe infranotificación al respecto. Debido a la gravedad de estas reacciones en personas previamente sanas, la decisión de prescribir quinolonas y fluoroquinolonas deberá tomarse tras realizar una cuidadosa evaluación de los beneficios y riesgos en cada paciente en concreto. Las fichas técnicas y prospectos de los medicamentos con quinolonas y fluoroquinolonas se actualizarán para incluir esta nueva información sobre seguridad. Se recuerda que las fichas técnicas y prospectos de los medicamentos con fluoroquinolonas también se han actualizado recientemente para incluir el riesgo de aneurisma y disección aórticos. Información adicional Para una información más detallada puede consultar la revisión realizada por la EMA a través del siguiente enlace: https://www.ema.europa.eu/en/medicines/human/referrals/quinolonefluoroquinolone-containing-medicinal-products
Asimismo, puede consultar la Nota Informativa publicada en la AEMPS sobre este tema: https://www.aemps.gob.es/informa/notasInformativas/medicamentosUsoHumano/seguridad/2018/ NI_MUH_FV-14-2018-quinolonas-fluoroquinolonas.htm
Fuente: Cofa
Lo más visto
- Covishield, la vacuna que India lanzó con Oxford-AstraZeneca
- El gobierno establece los requisitos para la producción de cannabis medicinal
- Anmat aprobó en el país la primera vacuna que protege contra el dengue
- Comunicación de Novo Nordisk: Diferencias en la indicación de Victoza® y Saxenda®
- Ibupirac declarado apto para celíacos