Mostrando artículos por etiqueta: COVID19
Avanza el estudio sobre el uso de Nitazoxanida para tratar el Covid-19
La nitazoxanida es un 5-nitrotiazol con actividad antiparasitaria y antibacteriana de amplio espectro. Este fármaco, derivado sintético de la sialicilamida, es efectivo contra una gran variedad de parásitos y bacterias, muchas de las cuales ocasionan síntomas como diarrea y otros malestares, que infectan tanto a animales como a seres humanos y se administra a través de comprimidos o por suspensión líquida.
Sin embargo, en la carrera por buscar nuevos tratamientos que puedan ayudar a reducir el agravamiento de los síntomas de COVID-19, el virus que ya ocasionó casi 148 millones de contagios en todo el mundo y provocó la muerte de 3,1 millones de personas, según los últimos datos del Johns Hopkins Medicine & University Resource Center, esta droga podría ser utilizada para tratar a los pacientes con coronavirus.
La nitazoxanida es una droga conocida en el mundo, que presenta escasos efectos adversos, generalmente leves y pasajeros, de tipo gastrointestinales. La medicación actúa fundamentalmente inhibiendo la expresión de una proteína viral denominada ‘N’ y también suprimiría la producción de citoquinas proinflamatorias, que se cree intervienen en el proceso de la enfermedad por COVID-19.
“La nitazoxanida es un antiparasitario que viene siendo utilizado hace mucho tiempo para distintas infecciones producidas por parásitos, pero también ha sido utilizado con éxito en distintas infecciones virales respiratorias, como la influenza, como el MERS y también a nivel de investigación clínica en hepatitis virales”, explicó Marcelo Silva, jefe de Hepatología del Hospital Universitario Austral.
Recientemente, el laboratorio estadounidense Romark, basado en Tampa, Florida, anunció los resultados iniciales de un ensayo clínico de Fase III de su nuevo fármaco candidato, nitazoxanida, en investigación NT-300 (tabletas de liberación prolongada de nitazoxanida, 300 mg) versus placebo como tratamiento para COVID-19 moderado. Basándose en los hallazgos, Romark está trabajando con la Administración de Drogas y Alimentos de los Estados Unidos (FDA) para solicitar una autorización de uso de emergencia en ese país.
Hoy, este antiparasitario se utiliza mayormente en adultos, aunque también puede ser utilizado en niños, para tratar infecciones por parásitos como ascaris y giardia lamblia. Esta última produce síntomas, que suelen aparecer de una a tres semanas después de la exposición a la enfermedad, y pueden incluir diarrea, fatiga, cólicos estomacales e hinchazón, gases, náuseas y pérdida de peso, explican desde la Mayo Clinic.
“Se trata de un antiparasitario muy bueno y eficaz contra protozoarios y gusanos intestinales; ya hace un tiempo surgió la posibilidad de probarlo en esta pandemia”, comentó el epidemiólogo Hugo Pizzi. Es que, según detalló el especialista, este fármaco se probó durante la epidemia de MERS-CoV, una enfermedad respiratoria vírica que se inició en abril de 2012 en Medio Oriente, provocada por otro coronavirus. “El virus del MERS es un coronavirus primo de este y además, en su momento, fue probada en patologías de vías aéreas superiores y cuadros gripales. Con el MERS disminuía citoquinas responsables del cuadro inflamatorio”, añadió.
La nitazoxanida fue evaluada contra un amplio rango de parásitos, incluyendo protozoos, nematodos, cestodos y trematodos, de modo de respaldar la evaluación clínica en humanos. “Se usa hace mucho para tratar parásitos o infecciones intestinales. El estudio está en Fase III y los resultados mostrarán su efectividad o no. Modificaría el rumbo de la enfermedad y evitaría agravamientos. Pero aún no se sabe. Es algo similar a lo que sucedía con la ivermectina”, en tanto, el médico pediatra Carlos Kambourian.
Estudios en la Argentina
La nitazoxadina está siendo investigada en la Argentina con prometedores resultados en un estudio clínico piloto con 135 pacientes con diagnóstico confirmado de COVID-19 y síntomas leves a moderados. El trabajo, que está publicado en el sitio internacional Clinical Trials, se está llevando adelante en el Hospital Universitario Austral y en la Clínica del Pilar de Ciudadela, ambos en la Provincia de Buenos Aires.
Silva, junto a su equipo de Investigación Clínica, había iniciado un estudio de eficacia y seguridad de este medicamento en el tratamiento de pacientes con infección por virus SARS-CoV2 (COVID-19) con síntomas leves o moderados a mediados del año pasado. El objetivo principal de la investigación fue el de evaluar si el medicamento evita la progresión de la enfermedad a estadios adonde se requiera la internación con asistencia intensiva.
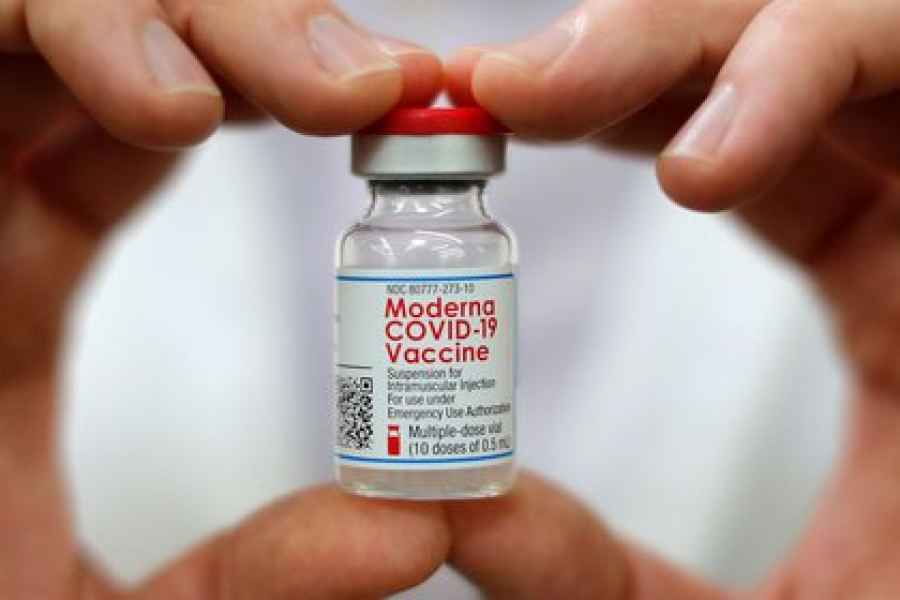
La OMS otorgó la autorización de emergencia a la vacuna de Moderna
La Organización Mundial de la Salud (OMS) otorgó este viernes su homologación de emergencia a la vacuna contra el covid-19 de la firma estadounidense Moderna. De esta manera, se convierte en el cuarto inoculante que obtiene esta luz verde del organismo de la ONU luego de que así lo hicieran los de Pfizer, AstraZeneca y Janssen (Johnson & Johnson).
Esta aprobación implica que las vacunas de Moderna pueden formar parte del programa COVAX, mediante el que la OMS distribuye dosis de vacunas -principalmente a países en desarrollo- y que hasta ahora mayoritariamente ha enviado vacunas fabricadas por AstraZeneca. Y también contribuye a que los países que no tienen medios para determinar si un medicamento es eficaz e inocuo, puedan acceder más rápidamente al mismo.
Previamente, la vacuna de Moderna, que al igual que aquella desarrollada por Pfizer usa la tecnología del ARN mensajero, había sido revisada por el Grupo Estratégico Asesor de Expertos, también ligado a la OMS, que ya había recomendado su uso en pacientes mayores de 18 años.
La OMS revisa estos días también el posible uso de emergencia de las vacunas chinas fabricadas por los laboratorios Sinopharm y Sinovac, aunque por ahora no ha emitido ninguna conclusión, pese a que los expertos de la organización iniciaron el estudio de los datos de la primera de ellas antes que los de Moderna.
La vacuna rusa Sputnik V, del laboratorio Gamaleya, también es tomada en consideración para un posible listado, aunque se encuentra en fases anteriores del proceso de homologación por parte de la OMS, a la espera de tener más datos para tomar la decisión de incluirla.
La vacuna de Moderna ha mostrado una eficacia del 94,1 % en pruebas de laboratorio y, según remarcó la OMS, puede mantenerse a temperaturas de entre 2 y 8 grados, similares a las de una nevera común, por lo que no necesita conservarse en ultrafrío, lo que facilita su distribución y almacenamiento.
La Administración de Alimentos y Medicamentos de los Estados Unidos emitió una autorización de uso de emergencia para la vacuna Moderna el 18 de diciembre de 2020 y la Agencia Europea de Medicamentos concedió una autorización de comercialización válida en toda la Unión Europea el 6 de enero de 2021.
Las autoridades de Moderna declararon el jueves que esperaban producir hasta 3.000 millones de dosis de su vacuna en 2022 mediante nuevos compromisos de financiación para impulsar el suministro en los centros de fabricación de Europa y Estados Unidos.
Pfizer prevé que su fármaco oral esté disponible para este año
El fármaco oral experimental de Pfizer para tratar el Covid-19 ante síntomas de la enfermedad podría estar disponible para fin de año, tal y como ha señalado este martes el director ejecutivo de la compañía, Albert Bourla, en una entrevista en la cadena CNBC.
Pfizer comenzó en marzo un ensayo clínico en fase 1 con un tratamiento antiviral oral contra el Covid-19. Este estudio, iniciado en Estados Unidos, analizaba la efectividad del PF-07321332, un inhibidor de la proteasa que ha demostrado tener una potente actividad antiviral in vitro. Los inhibidores de la proteasa se utilizan para tratar otros patógenos virales como el VIH y la hepatitis C.Si los ensayos clínicos van bien y la FDA lo aprueba, el medicamento podría distribuirse en los EEUU antes de fin de año, ha señalado Bourla.
Los expertos confían en que el medicamento, que se toma por vía oral, constituya una herramienta clave para combatir al Covid-19 ya que las personas recién infectadas podrían usarlo fuera de los hospitales.
Covid: Vacuna Pfizer para niños
Además de este medicamento, Pfizer está probando su vacuna en niños de 6 meses a 11 años. A principios de este mes, la compañía le pidió a la FDA que expandiera su autorización de vacuna a adolescentes de 12 a 15 años después de que un estudio señalara que la inyección es 100 por 100 efectiva.
En este sentido, Bourla se ha mostrado muy optimista de que la FDA aprobará el uso de la inyección en adolescentes.
Crecen en la Argentina las internaciones en menores de 60 años
En lo que va de abril de 2021, el 56,3 por ciento de los internados en terapia intensiva en hospitales nacionales de Argentina son menores de 60 años, en línea con la tendencia que se viene registrando en otros países de la región durante 2021, tal como informó ayer la Organización Panamericana de la SALUD (OPS).
De ese porcentaje, el 43,8 % corresponde a mayores de 60 años, el 44,8 % al grupo de entre 40 a 60 y el 11,5 % al grupo entre 15 y 40 años. Además, en terapia intermedia la situación se repite con un 40 % de ocupación de mayores de 60; un 50,7 % correspondiente al grupo etario de entre 40 y 60 y 9,3 % al grupo entre 15 y 40 años.
El patrón coincide con los resultados de un estudio de la Sociedad Argentina de Terapia Intensiva (SATI) que arrojó “una alta ocupación de camas a predominio de pacientes jóvenes graves portadores de la COVID-19, con un alto requerimiento de asistencia respiratoria mecánica y de posición prono” (boca abajo).
El estudio se basa en una encuesta a nivel nacional del 16 de abril en la que participaron 163 unidades de terapia intensiva (52% públicas y 48% privadas), y que representan 3.332 camas a nivel país. El promedio de edad de los pacientes internados el día del estudio fue de 53 ± 8 años, indicó la SATI.
Sin embargo, en cuanto a la mortalidad, en Argentina el grupo de edad más afectado continúa siendo el de 60 años y más, con un aumento de la tasa de letalidad conforme aumenta la edad. El 83,3 % de los fallecidos en 2021 correspondió a mayores de 60 años.
“Casi el 60 % de los internados en terapia son menores de 60 años, pero en los fallecidos vemos que siguen siendo los mayores de 60 años”, precisó la directora nacional de Epidemiología del ministerio de Salud, Analía Rearte. “Todavía tenemos para un par de semanas más de tensión, esta disminución es muy incipiente”, agregó.
La situación en otros países de la región
En un alerta epidemiológica de ayer, la Organización Panamericana de la Salud (OPS/OMS) indicó que si bien el número de hospitalizaciones, de internaciones en unidades de terapia intensiva (UTI) y de defunciones por COVID-19 eran más altas en adultos mayores y en aquellas personas con comorbilidades, “a nivel global se observa un cambio del perfil de la edad de los casos hospitalizados, y hospitalizados en UTI, con una mayor tasa de hospitalización en población más joven”.
A nivel regional, el alerta de la OPS menciona los casos de Brasil, Chile, Paraguay y Perú en los que se registra “el incremento de severidad en población menor de 60 años”.
Según el informe, en Brasil cuando se compara la tasa de hospitalización más alta ocurrida en 2020 (13 de julio) con la tasa más alta ocurrida en 2021 (10 de marzo) se observa que los menores de 39 años, y los grupos de 40-49 años así como los de 50-59 años duplicaron el valor de las tasas de hospitalización. El mayor incremento porcentual se registró en el grupo de 40-49 años (56 %), seguido por los menores de 39 años (53 %) y el grupo de 50-59 años (51 %). Entre los adultos mayores de 60 años el incremento fue menor con 32 %.
Respecto de las tasas de mortalidad, el informe de OPS señala que en Brasil se observa un incremento desde inicios de diciembre de 2020 en todos los grupos etarios, y que se mantiene la mayor tasa de mortalidad en los adultos mayores en un rango que osciló entre 1,8 por 100.000 habitantes y 142,7 por 100.000 habitantes (marzo 2021). En los menores de 39 años el rango es de 0,0 a 2,9 por 100.000 habitantes; mientras que en el grupo de 40-49 años de 0,2 a 19,4 por 100.000 habitantes en y en el grupo de 50-59 años de 0,3 a 41,6 por 100.000 habitantes.
Sin embargo, al comparar las tasas de mortalidad registradas en diciembre 2020 con las de marzo 2021, se observa que mientras en los adultos mayores se duplicó, en los menores de 39 años y en el grupo de 40-49 años se cuadruplicó mientras que en el grupo de 50-59 años se triplicó.
La situación se replica en Chile, en el que si bien las tasas de ocupación diaria de las camas de UTI muestran que entre abril y diciembre de 2020, a mayor edad, mayor tasa de hospitalización, desde mediados de marzo de 2021 en adelante se observa un cambio en ese patrón. Así el grupo de 50-59 años presentó una tasa mayor que la de los adultos mayores.
Además, en los menores de 49 años la tasa se triplicó con incrementos de 71 % y 65% en los menores de 39 años y en el grupo de 40-49 años respectivamente; mientras que en el grupo de 50-59 años la tasa se duplicó. Por otro lado, en el mismo periodo, el grupo de mayores de 60 años presentó un descenso de 8 % en la tasa de hospitalización en UTI.
Al comparar las tasas de mortalidad registradas en diciembre 2020 con las tasas registradas en marzo 2021, se observó que todos los grupos etarios las duplicaron y que los mayores incrementos porcentuales se observaron en los grupos de 50-59 años (60%) y en los menores de 39 años (59%).
En Paraguay las tasas de mortalidad de marzo de 2021 son las más altas registradas desde las primeras defunciones ocurridas en ese país, en todos los grupos etarios.
Luego, al comparar las tasas de mortalidad de diciembre 2020 con las tasas de marzo 2021, en Paraguay se observó que los grupos etarios de 50-59 años y de mayores de 60 años las tasas se duplicaron, en tanto que en los menores de 39 años la tasa de mortalidad se triplicó y en el grupo de 40-49 años se quintuplicó.
Finalmente, en Perú al comparar las tasas de mortalidad registradas en diciembre 2020 con las tasas registradas en marzo de 2021, se observó que tanto en los menores de 39 años y en los de 60 y más las tasas se triplicaron con un incremento relativo de 66 y 67 % respectivamente. Mientras que los grupos de 40-49 años y de 50-59 años esas tasas se cuadruplicaron e incrementaron en 73% y 77% respectivamente.
Sputnik V: Richmond mandó las primeras dosis de prueba a Rusia
El laboratorio Richmond informó hoy ante la Comisión Nacionales de Valores (CNV) que está finalizando la elaboración de los primeros lotes de prueba de la vacuna Sputnik V contra el coronavirus. “Estos lotes están siendo enviados al Gamaleya Center [el instituto que desarrolló la vacuna rusa] para su evaluación, mientras que otros ensayos son realizados en paralelo en nuestros laboratorios”, dice la nota.
Según ampliaron luego en un comunicado, está previsto que la producción a gran escala de la Sputnik V en el país comience en junio. La Argentina fue el primer país de América Latina en registrar oficialmente la vacuna en su territorio. El registro se llevó a cabo a través de una autorización de uso de emergencia y la vacunación comenzó el 29 de diciembre de 2020.
“La vacuna producida en la Argentina podrá ser exportada a otros países de América Central y América Latina”, señalaron en un comunicado. En el día, el precio de las acciones de la empresa subió más de 23%.
Actualmente, la Sputnik V está registrada en 60 países, que suman una población total de 3000 millones de personas. La efectividad de la vacuna es del 97,6%, según el resultado del análisis de datos sobre la incidencia del coronavirus entre los rusos vacunados con ambos componentes en el período comprendido entre el 5 de diciembre de 2020 y el 31 de marzo de 2021.
En febrero pasado, el laboratorio que preside Marcelo Figueiras anunció que firmaba un memorándum de entendimiento entre Management Company of Russian Direct Investment Fund -Fondo Ruso de Inversión Directa (RDIF)-, quien representa a Gamaleya National Research Institute of Epidemiology and Microbiology, para fomentar la cooperación entre las partes y así poder fabricar la vacuna en la Argentina.
“Nuestro país es el primero de Latinoamérica en comenzar el proceso de transferencia tecnológica de la vacuna Sputnik V, todo lo cual fue posible gracias a la colaboración de RDIF y de sus socios estratégicos”, dice el comunicado.
“De no mediar dificultades, a la mayor brevedad posible, se comenzaría con la etapa de producción de la Sputnik V en la República Argentina”.
“Laboratorios Richmond se enorgullece del apoyo de RDIF, que confió en nuestra base científica y tecnológica para producir la vacuna Sputnik V en la Argentina. Nuestra empresa hará todo lo posible para garantizar que la vacuna esté disponible lo antes posible para la Argentina y para toda la región de América Latina”, dijo Figueiras.
Kirill Dmitriev, director ejecutivo RDIF, declaró: “La Argentina fue la primera en América Latina en aprobar el uso de la vacuna Sputnik V y comenzar a vacunar a la población. Hoy nos complace anunciar que la Argentina también se ha convertido en el primer estado de la región en iniciar la producción de Sputnik V gracias a la asociación entre RDIF y Laboratorios Richmond. Sputnik V está aprobada en más de 10 países de América Latina y Centroamérica, y la producción en la Argentina permitirá realizar las entregas a nuestros otros socios”.
La semana pasada, la empresa anunció que creaba el fideicomiso financiero llamado “Proyecto Vida” (Vacuna de Inmunización para el Desarrollo Argentino) para construir una planta en Pilar, donde se produciría en un año la vacuna Sputnik V. El laboratorio todavía busca recaudar US$70 millones.
“Se hizo un gran trabajo y en tiempo récord para lanzar el fideicomiso Proyecto Vida. Estamos convocando al mercado de capitales para construir esta planta que permitirá producir las vacunas para paliar esta pandemia y sus mutaciones. Es el camino más eficiente, eficaz y sustentable, ya que nos fortalece en autonomía y capacidad de reacción frente al virus”, había dicho Marcelo Figueiras, presidente de Richmond, durante la presentación vía Zoom.
Según explicó, firmaron un convenio con el fondo que representa al Instituto Gamaleya para producir la Sputnik V, pero el proyecto incluirá la fabricación de productos de biotecnología, como anticuerpos monoclonales, y también puede ser la base de producción para otras compañías.
“Estamos convencidos de que un mayor desarrollo del país permitirá no depender solamente de los países centrales frente a situaciones como la actual. Tiene que haber una industria fuerte con muchos jugadores para asistir también a otros mercados y, a este efecto, el mercado de capitales local debe jugar un rol fundamental”, señaló.
Jóvenes y Covid-19
El contagio de coronavirus ofrece cierta protección a los jóvenes, pero no garantiza una completa inmunidad contra la reinfección, advierte un estudio publicado en la revista The Lancet Respiratory Medicine.
La investigación basada en datos de más de 3.000 miembros sanos del Cuerpo de Marines de Estados Unidos, la mayoría de los cuales eran hombres de entre 18 y 20 años concluye que, aunque se desarrollen anticuerpos tras superar la enfermedad, es conveniente recibir la vacuna para estimular la respuesta inmunitaria y evitar reinfecciones.
Para el estudio, desarrollado entre mayo y noviembre de 2020, los reclutas completaron una cuarentena de cuatro semanas antes de regresar a los entrenamientos, se sometieron a pruebas para detectar anticuerpos y contagios y rellenaron un cuestionario sobre síntomas de COVID-19, entre otros datos médicos.
Según la investigación, de tipo “observacional”, diecinueve jóvenes (10%) de 189 que ya habían superado el coronavirus se infectaron de nuevo, mientras que en el grupo de los que no habían contraído el virus, integrado por 2.247 participantes, se contagiaron posteriormente 1.079, casi la mitad.
Los autores constataron que las personas que nunca se habían infectado tenían hasta cinco veces más riesgo de contagiarse que aquellos que ya habían pasado la enfermedad, aunque estos últimos no eran completamente inmunes.
El infectólogo Lautaro de Vedia, ex presidente de la Sociedad Argentina de Infectología, aseguró: “La investigación confirma algo que ya suponíamos. La gente que tuvo COVID-19, si bien con una tasa mucho menor que los que no habían tenido, algunos se infectaron (un 10% versus un 50% del otro grupo). Haber transitado la infección te genera cierto nivel de anticuerpos sin duda, pero no te convierte en inmune. Las vacunas son lo que van a dar fin a esta pandemia”.
Los científicos sostienen que los jóvenes reinfectados tenían menos anticuerpos que los participantes que no habían vuelto a contraer el virus y su carga viral era “sólo” diez veces más baja que la de aquellos reclutas que se habían contagiado por primera vez.
De acuerdo con los autores, esto significa que alguna personas reinfectadas pueden transmitir el virus, aunque es una conclusión que, advierten, requiere más investigación para poder confirmarse.
Ante estos datos, los científicos alientan a los jóvenes a aceptar inmunizarse cuando llegue su turno para asegurar su protección frente a la enfermedad, aun cuando hayan tenido la enfermedad anteriormente.
“A medida que las campañas de vacunación siguen ganando impulso, es importante recordar que, a pesar de una infección previa por COVID-19, los jóvenes pueden contraer el virus nuevamente y pueden transmitirlo a otras personas”, señala en un comunicado uno de los autores del estudio, Stuart Sealfon, de la estadounidense Escuela de Medicina Icahnde Monte Sinaí.
El SARS-CoV-2 no ha afectado clínicamente a los adolescentes de forma grave en comparación con otros grupos, sin embargo, se han visto profundamente afectados por las medidas de control, por ejemplo, el distanciamiento social y el cierre de escuelas.
En la mayor parte del mundo, la respuesta a la pandemia de COVID-19 ha sido “guiada por la ciencia”. Ahora, las consecuencias psicosociales y económicas más amplias de la pandemia están emergiendo rápidamente. Aunque los jóvenes han sufrido menos que otros grupos vulnerables como resultado directo de la enfermedad, el impacto indirecto sobre ellos ha sido marcado. Quizás -advierte una investigación publicada en la prestigiosa revista científica British Medical Journal (BMJ)- de mayor preocupación son los efectos educativos y psicosociales del distanciamiento físico, el aislamiento social y el cierre de escuelas en el bienestar de los niños.
Cuba, a un paso de lograr la primera vacuna latinoamericana
Se llaman Soberana 02 y Abdala, y son los dos candidatos vacunales cubanos contra la covid-19 que más lejos han llegado en su desarrollo. Ambos están en fase 3 de ensayos clínicos, la última antes de su aprobación y si todo sale ―como esperan los científicos cubanos― antes de terminar el verano, la isla podría disponer de una vacuna propia con la que inmunizar a toda su población, de 11,2 millones de habitantes. De lograr la aprobación de la Agencia Nacional Reguladora de Cuba, algo que parece muy probable, Soberana 02 y Abdala se convertirán en los próximos meses en las primeras vacunas anticovid concebidas y producidas en América Latina.
La Organización Panamericana de la Salud (OPS) considera todo un lujo y un “privilegio” que un pequeño país como Cuba haya logrado desarrollar cinco candidatos de vacunas, y que dos se encuentren en la última etapa de ensayos clínicos, en la que se prueba su eficacia. “No se trata de ningún milagro: existe un notable desarrollo científico en Cuba y una experiencia de 30 años en fabricar vacunas”, dijo en una reciente entrevista con EL PAÍS el representante en Cuba de la OPS/OMS, José Moya, quien destacó que no es casualidad que la isla fuera el primer país en desarrollar una vacuna antimeningocócica, además de fabricar —a comienzos de los noventa— otra contra la hepatitis b que fue ampliamente empleada en América Latina y África.
Todos los prototipos cubanos se basan en inocular una proteína de la espícula del coronavirus, la parte que se une a las células que infecta, para producir una respuesta inmunológica. Soberana 02, en la que más expectativas hay depositadas, añade además un potenciador de la respuesta inmune. Cuba ya ha desarrollado con éxito otra vacuna con este principio contra la bacteria Haemophilus influenzae b responsable de algunas meningitis y neumonías.
Según Moya, los científicos cubanos están trabajando sobre plataformas conocidas y eso siempre es una seguridad. “Este tipo de vacunas son las más tradicionales y seguras, además de tener la ventaja de que se conservan a una temperatura de dos a ocho grados”, indicó el epidemiólogo peruano, que considera una fortaleza de Cuba poseer una agencia reguladora sólida y de referencia en América Latina, como es el Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos, con el que la OPS colabora desde hace años. Es esta agencia la que finalmente decidirá si Soberana 02 y Abdala se convierten en vacunas y se autoriza su uso de emergencia antes de que concluyan todas las pruebas.
Ensayos con voluntarios
El pasado 3 de abril concluyó la aplicación de la primera dosis de Abdala en 48.000 voluntarios de las provincias orientales de Santiago de Cuba, Guantánamo y Granma, y el 5 de abril comenzó a ponerse la segunda inyección de esta vacuna, de la que se administrarán tres dosis (0, 14 y 28 días) en dos grupos, uno experimental y otro de control. El 5 de abril se inició también la aplicación de la segunda dosis de Soberana 02 a los cerca de 42.000 voluntarios incluidos en el ensayo fase III en La Habana. Soberana 02 fue el primer candidato anticovid-19 de la isla que llegó a la última etapa de ensayos, pero con un esquema más largo de inyecciones: a los 0, 28 y 56 días.
De los laboratorios de BioCubaFarma, entidad a la que pertenecen 32 institutos, centros de investigación e industrias de producción biotecnológica y farmacéutica, ya han salido más de 300.000 dosis de Soberana 02 y Abdala, y sus directivos aseguran que tienen capacidad para producir 100 millones de viales antes de que termine 2021. El objetivo declarado es tener al menos una vacuna lista en verano y empezar la vacunación masiva en julio y agosto. Se pretende tener inmunizada a la mitad de la población en septiembre y a todos los cubanos antes de que finalice el año.
“Los resultados hasta ahora son alentadores: ambos candidatos vacunales han demostrado ser seguros y capaces de generar anticuerpos específicos contra el virus. Somos optimistas”, declaró poco antes de comenzar la fase III Eulogio Pimentel, vicepresidente del grupo empresarial BioCubaFarma, que produce ocho de las 13 vacunas que forman parte del programa nacional de vacunación de la isla.
Los cinco candidatos cubanos contra la covid-19 —todos de nombres patrióticos— son: Soberana 01, Soberana 02 y Soberana Plus (concebida para aplicarse a convalecientes de covid-19, actualmente en fase 2 de ensayos clínicos), que son desarrollados por el Instituto Finlay; y Abdala y Mambisa (que tiene la peculiaridad de ser administrada mediante un espray nasal), del Centro de Ingeniería Genética y Biotecnología.
Para Cuba, coronar con éxito el desarrollo de sus vacunas es de crucial importancia. En primer lugar, por el prestigio científico y político que representa, pero también por motivos económicos en momentos en que la isla atraviesa una de las peores crisis de su historia, y cuando la epidemia de coronavirus está en su peor momento (una media de 1.000 casos diarios en los últimos días), y no existen planes de adquirir ninguna vacuna extranjera.
Cuba pretende exportar su vacuna, y ya algunos países del área han expresado su interés. Venezuela anunció la semana pasada que se dispone a fabricar en un laboratorio de Caracas la vacuna Abdala, todavía en fase de pruebas, en cooperación con el Gobierno de La Habana. También Jamaica y Surinam, entre otros países del Caricom (Comunidad del Caribe), han mostrado su interés en acceder a las vacunas cubanas cuando estén listas.
ANMAT aprobó la venta en farmacias de un test rápido de Covid-19
La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) autorizó la venta en farmacias de un test rápido de coronavirus.
El producto en cuestión es de origen chino, se conoce como Immunobio, y su desarrollo estuvo en manos del laboratorio Hangzhou Immuno Biotech CO Ltd. Es importante mencionar que se trata del único autorizado por la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) para su venta en farmacias.
El test rápido de coronavirus permite conocer el resultado en aproximadamente 10 minutos. Ese resultado tiene una efectividad del 96,8%. De todas maneras, es muy importante estar atentos a la advertencia que el propio envase brinda.
Allí se aclara que en caso de dar negativo esto no descarta una posible presencia del virus en la persona testeada. “Los resultados negativos no descartan infección por Covid-19”, dice.
Es importante tener en cuenta que el test rápido no es para que las personas vayan por su cuenta, lo compren y lo hagan en sus casas. Se trata de una prueba que, si bien está autorizada a venderse en farmacias, es de uso profesional exclusivo. Esto significa que debe ser un profesional de la salud quien realice el test a la persona que crea tener coronavirus o que necesite saber su estado de salud.
Se trata de un test de antígeno que se hace a través de un hisopado “para la detección cualitativa de antígenos del nuevo coronavirus SARS-CoV2 utilizando secreciones de garganta humana y secreciones nasales. El mismo está compuesto por una bolsa de aluminio con cassete de prueba y desecante, tampón de ensayo (buffer), hisopo estéril y tubo de recolección de muestras e instrucciones de uso”.
¿Vitamina D para tratar Covid -19?
La búsqueda de herramientas para encontrar más tratamientos contra el COVID-19 no se ha frenado desde el inicio de la pandemia. Uno de los productos que se ha postulado es la vitamina D, que ha llamado la atención de investigadores científicos de diferentes partes del mundo. Las pruebas sobre la utilidad de la vitamina D para el coronavirus aún está en debate. En la Argentina y en Inglaterra, avanzan estudios para arrojar pistas que permitan dilucidar si la vitamina D puede ser incluida en la lista de suplementos que pueden ayudar en los afectados por el coronavirus.
Además de promover una buena salud ósea, la vitamina D puede desempeñar algunas funciones para ayudar al funcionamiento de las células inmunitarias. Algunos estudios científicos encontraron el año pasado una asociación entre los bajos niveles de vitamina D y las tasas elevadas del COVID-19. Sin embargo, esos trabajos no han podido determinar que esta deficiencia en la vitamina D sea la causa real de las tasas de la enfermedad. Podría estar ocurriendo que las poblaciones que tienen mayor deficiencia de vitamina D resulten más afectadas por el coronavirus por otros motivos, como por ejemplo un menor acceso a los servicios de salud o condiciones preexistentes como la obesidad.
También hubo ensayos clínicos que han intentado determinar si la vitamina D puede ayudar a los pacientes con COVID-19. La posibilidad recibió más atención cuando el 2 de octubre pasado se conoció que el ex presidente de los Estados Unidos, Donald Trump, recibió vitamina D cuando fue diagnosticado con COVID-19. En Inglaterra, la vitamina D se recomienda para su consumo al comienzo del invierno. Pero hasta ahora, ninguna investigación ha demostrado un efecto lo suficientemente contundente como para respaldar dosis más altas para prevenir o tratar el coronavirus.
Varios estudios han demostrado una asociación entre la vitamina D y los resultados de COVID-19, pero son en gran medida observacionales. Esto significa que analizan lo que ocurre con las personas con niveles más altos y más bajos de vitamina D, pero no se controlan otros factores. Los estudios observacionales muestran que ciertos grupos son más propensos a tener deficiencias de vitamina D y a contraer Covid: las personas mayores, las personas con obesidad, y las personas con piel más oscura.
Es posible que una deficiencia en la vitamina D sea la razón por la que estos grupos tienen un mayor riesgo, o puede haber otros factores de salud y ambientales que provoquen tanto una caída de niveles de vitamina D como una mayor susceptibilidad al coronavirus.
Pero también es posible que los niveles de la vitamina D también pueden descender como consecuencia de la enfermedad y que no sean la causa.
Para aclarar cuál es el rol de la vitamina D, se esperan los resultados de varios estudios en curso. Un ensayo controlado y aleatorizado se está llevando a cabo en la Universidad Queen Mary de Londres. Otro ensayo se está realizando en Argentina con financiamiento del Ministerio de Ciencia, Tecnología e Innovación.
Según contó a Infobae el doctor Walter Manucha, investigador del Instituto de Medicina y Biología Experimental de Cuyo del Conicet en Mendoza, se está haciendo un ensayo controlado multicéntrico con vitamina D en altas dosis versus placebo para prevenir las complicaciones evolutivas de pacientes infectados por COVID-19. Se les administra un grupo de pacientes leves a moderados con la vitamina D y otro grupo solo recibe placebo.
El ensayo fue uno de los 64 elegidos por una convocatoria de la Agencia Nacional de Promoción de la Investigación, el Desarrollo Tecnológico y la Innovación, que depende del Ministerio de Ciencia. El estudio intenta comprobar si las altas dosis de vitamina D3 (colecalciferol) reduce el riesgo de mayores complicaciones en los pacientes leves y moderados. Se intenta averiguar si la elevación en forma rápida y sostenida de los niveles de vitamina D en sangre puede morigerar la situación de estos pacientes y mejorar rápidamente la respuesta del organismo frente a la infección.
Otra pista fue dada por otro estudio -aún sujeto a revisión de pares-, que fue realizado por un equipo internacional de investigadores de la Universidad de Nueva York, Instituto de Cáncer Barts Cancer, de Londres, entre otros-. Sugirió que las tasas de mortalidad por COVID-19 son menores en los países con una exposición anual al sol más insuficiente, pero con niveles medios de vitamina D más altos. Este trabajo señala que se necesitan resultados de ensayos clínicos controlados que permitan aclarar si hay relación entre el consumo de vitamina D y COVID-19
El año pasado, hubo un estudio de la Universidad de Barcelona que capturó la atención. Sugirió que la vitamina D había tenido un éxito asombroso, con una reducción del 80% de los ingresos en cuidados intensivos y una reducción del 60% de las muertes por Covid. Fue ampliamente compartido en Internet. Pero luego fue retirado por “preocupaciones sobre la descripción de la investigación”, y la revista The Lancet inició una investigación sobre ese trabajo.
Butanvac: la primer vacuna brasileña contra el Covid-19
Brasil está a las puertas de empezar a probar en humanos una vacuna desarrollada por el estatal Instituto Butantán. Es una noticia que podría cambiar el desarrollo de la pandemia en América Latina, una región donde el avance del Covid-19 vuelve a acelerarse en varios países. Por ese crecimiento en el número de contagios, Argentina suspendió los vuelos con Brasil, Chile y México. En otras noticias, Alemania clasificó a Francia como “zona de alto riesgo”.
La pandemia de Covid-19 sigue avanzando en todo el mundo, mientras los países tratan de acelerar sus campañas de vacunación y buscar recursos para combatirla. Por ejemplo, Brasil anunció su primera vacuna desarrollada en el país, una vacuna que tendrá como objetivo distribuirse en el sur global y en los países con más dificultades para asegurar los fármacos. Otros países siguen, mientras tanto, aumentando las restricciones para evitar que los contagios crucen más fronteras. Alemania declaró a toda Francia como zona de alto riesgo de infección de Covid-19 y Argentina suspendió sus vuelos regulares con Brasil, México y Chile.
El gobernador de Sao Paulo, Joao Doria, anunció que el Instituto Butantán, una institución pública brasileña, ha desarrollado su propia vacuna, la Butanvac. El fármaco está a la espera de la aprobación de las entidades reguladoras del país para empezar a probarse en humanos. Es un anuncio histórico para el mundo. La vacuna 100 % nacional, con pruebas prometedoras y fruto del trabajo de una institución de 120 años de su existencia, que es el mayor productor de vacunas del Hemisferio Sur, recordó Doria en una rueda de prensa desde Sao Paulo.
Joao Doria, una de las caras de la lucha contra la pandemia en Brasil y fuerte opositor del presidente Jair Bolsonaro, anunció que espera empezar la inoculación con el fármaco Butanvac en julio, una fecha ambiciosa.
El objetivo del Instituto Butantán es producir 40 millones de dosis este año a partir de mayo, con el objetivo de contribuir a la campaña de vacunación brasileña, que por ahora se desarrolla con lentitud. La Butanvac está diseñada para inmunizar contra la variante P1 del Covid-19, la variante encontrada en el estado del Amazonas que disparó una fuerte segunda ola de contagios en Brasil y que ya ha llegado a la mayoría de países del continente.
El Butantán ya ha producido 27,8 millones de dosis de la vacuna china CoronaVac, la base de la campaña de vacunación de Brasil, a través de un acuerdo con Sinovac. El director del Instituto, Dimas Covas, aseguró que el desarrollo de la nueva vacuna no interferirá con la producción del otro fármaco.
La producción de este medicamento podría suponer un cambio a corto pero sobre todo a mediano plazo en la geopolítica sanitaria que ha venido de la mano de la pandemia. Según Covas, el objetivo de la Butanvac es ofrecerla para países de renta baja y media, que es donde necesitamos combatir la pandemia. Según el director del Instituto Butantán, su vacuna podría ser una gran contribución y va a ser la diferencia en el curso de la epidemia y nos va a ayudar a combatirla en todo el mundo.
Lo más visto
- Covishield, la vacuna que India lanzó con Oxford-AstraZeneca
- El gobierno establece los requisitos para la producción de cannabis medicinal
- Anmat aprobó en el país la primera vacuna que protege contra el dengue
- Comunicación de Novo Nordisk: Diferencias en la indicación de Victoza® y Saxenda®
- Ibupirac declarado apto para celíacos