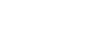Mostrando artículos por etiqueta: AstraZeneca
Un fármaco de AstraZeneca reduce las muertes por Covid-19 hasta un 67%
El fármaco AZD7442 de Astrazeneca, una combinación de anticuerpos de acción prolongada (LAAB), reduce hasta un 67 por ciento los casos de Covid-19 grave o muerte en pacientes con cinco días de síntomas, según los resultados de un ensayo de fase III.
El ensayo cumplió el criterio de valoración principal, ya que una dosis de 600 mg de AZD7442 administrada por inyección intramuscular redujo el riesgo de desarrollar Covid-19 grave o muerte (por cualquier causa) en un 50 por ciento en comparación con el placebo en pacientes ambulatorios que habían estado sintomáticos durante siete días o menos. El LAAB fue generalmente bien tolerado en el ensayo. El 90 por ciento de los participantes inscritos pertenecían a poblaciones con alto riesgo de progresión a la Covid-19 grave, incluidos aquellos con comorbilidades.
AZD7442 es el primer LAAB con datos de fase III que demuestra su beneficio tanto en la profilaxis como en el tratamiento de la Covid-19 y se administra fácilmente mediante inyección intramuscular.
Con los continuos casos de infecciones graves por Covid-19 en todo el mundo, existe una importante necesidad de nuevas terapias como AZD7442 que puedan utilizarse para proteger a las poblaciones vulnerables de contraer este virus y que también puedan ayudar a prevenir la progresión a la enfermedad grave. Estos resultados positivos muestran que una cómoda dosis intramuscular de AZD7442 podría desempeñar un papel importante para ayudar a combatir esta devastadora pandemia, asegura Hugh Montgomery, catedrático de Medicina Intensiva en el University College de Londres (Reino Unido) e investigador principal de ‘TACKLE’.
Estos importantes resultados de AZD7442, nuestra combinación de anticuerpos de acción prolongada, se suman al creciente cuerpo de evidencia para el uso de esta terapia tanto en la prevención como en el tratamiento de la Covid-19. Una intervención temprana con nuestro anticuerpo puede proporcionar una reducción significativa de la progresión hacia la enfermedad grave, con una protección continuada durante más de seis meses, detalla el vicepresidente ejecutivo de I+D de Biofármacos de Astrazeneca, Mene Pangalos.
La compañía ha anunciado que discutirá estos datos con las autoridades sanitarias. El 5 de octubre, Astrazeneca avanzó que había presentado una solicitud a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) para la autorización de uso de emergencia de AZD7442 para la profilaxis de la COVID-19. Además, los resultados completos de ‘TACKLE’ se enviarán para su publicación en una revista médica revisada por expertos y se presentarán en una próxima reunión médica.
‘TACKLE‘ es un ensayo multicéntrico de fase III, aleatorizado, doble ciego y controlado con placebo, que evalúa la seguridad y la eficacia de una dosis única de 600 mg de AZD7442 por vía intramuscular en comparación con un placebo para el tratamiento ambulatorio de la Covid-19. El ensayo se llevó a cabo en 96 centros de Brasil, República Checa, Alemania, Hungría, Italia, Japón, México, Polonia, Rusia, España, Ucrania, Reino Unido y Estados Unidos. Se aleatorizó a 903 participantes para que recibieran AZD7442 o placebo salino, administrados en dos inyecciones intramusculares separadas y secuenciales.
Los participantes eran adultos de 18 años o más que no estaban hospitalizados con Covid-19 de leve a moderada y con síntomas durante siete días o menos. Los participantes tenían una infección de SARS-CoV-2 documentada y confirmada por el laboratorio, determinada por una prueba molecular (antígeno o ácido nucleico) de cualquier muestra del tracto respiratorio (por ejemplo, hisopo orofaríngeo, nasofaríngeo o nasal o saliva) recogida no más de tres días antes del primer día.
Aproximadamente el 13 por ciento de los participantes tenían 65 años o más. Además, el 90 por ciento tenía comorbilidades de base y otras características que los ponían en alto riesgo de progresión a Covid-19 grave, incluyendo cáncer, diabetes, obesidad, enfermedad pulmonar crónica o asma, enfermedad cardiovascular o inmunosupresión.
AZD7442 es una combinación de dos LAAB, tixagevimab (AZD8895) y cilgavimab (AZD1061), derivados de células B donadas por pacientes convalecientes del virus del SARS-CoV-2. Descubiertos por el Centro Médico de la Universidad de Vanderbilt y licenciados a AstraZeneca en junio de 2020, estos anticuerpos monoclonales humanos se unen a sitios distintos de la proteína de espiga del SARS-CoV-21 y fueron optimizados por Astrazeneca.
La prolongación de la vida media triplica la duración de su acción en comparación con los anticuerpos convencionales y podría proporcionar hasta 12 meses de protección frente a la Covid-19 tras una única administración. De hecho, los datos del ensayo de fase I muestran títulos elevados de anticuerpos neutralizantes durante al menos nueve meses.
La EMA abre la puerta a combinar la vacuna de AstraZeneca y Pfizer
La Agencia Europea del Medicamento (EMA, por sus siglas en inglés) abre la puerta por primera vez a combinar la vacuna contra la Covid-19 de AstraZeneca con una segunda dosis de Pfizer-BioNTech, como hace España. La ministra de Sanidad, Carolina Darias, ha adoptado esta fórmula para los menores de 60 años con el fin de minimizar el riesgo de casos raros de trombos.
No obstante, la recomendación central de la EMA sigue siendo administrar la segunda dosis de AstraZeneca a los que ya han recibido la primera, independientemente de su edad, según ha explicado su responsable de estrategia de vacunación, Marco Cavaleri. Una opción por la que están apostando también la mayoría de los españoles, desoyendo la recomendación de Sanidad.
“Es un tema muy importante que se está discutiendo ahora mismo“, ha respondido Cavaleri este viernes en una rueda de prensa.
“Por lo que hemos escuchado hasta ahora, estos datos muestran que no hay preocupaciones importantes sobre esta estrategia desde el punto de vista de la seguridad. Y por el lado de la inmunogenicidad, se trata realmente de un enfoque eficaz para generar una respuesta inmune robusta tras la segunda dosis de una vacuna diferente”, sostiene Cavaleri.
“No obstante, queremos recoger más pruebas y vamos a examinar todos estos estudios con el objetivo de garantizar que este enfoque es tan bueno como parece”, ha añadido.
Hasta este momento, la EMA había aconsejado inocular la segunda dosis de AstraZeneca a todas las personas que ya han recibido la primera inyección de esta marca, independientemente de su edad, por considerarlo la opción más segura. ¿Cambiará esta recomendación? “En efecto, la recomendación respecto a la vacuna de AstraZeneca es dar la segunda dosis. Ahora hay una contraindicación para los que sufrieron una trombosis tras la primera dosis, pero este es el único cambio. La recomendación sigue siendo la misma”, ha señalado Cavaleri.
Eso sí, el regulador europeo no descarta usar una vacuna diferente en la segunda dosis, como hace España. Una alternativa que había rechazado en un primer momento por falta de datos suficientes.
Según el análisis de la EMA, los casos raros de trombosis afectan a 1 de cada 100.000 personas vacunadas con AstraZeneca. Los beneficios de esta inyección a la hora de prevenir los casos de hospitalización y muerte por Covid-19 superan ampliamente a los riesgos de efectos secundarios. Unos beneficios que aumentan con el incremento de la edad y de las tasas de infección.
El regulador europeo no ha dado indicaciones claras sobre los beneficios y riesgos en función del sexo, aunque en un primer momento señaló que los coágulos afectan sobre todo a mujeres menores de 60 años.
Combinar vacunas distintas aumentaría la posibilidad de padecer efectos secundarios
Como parte de la lucha que llevan adelante los gobiernos para dar batalla a la pandemia de COVID-19, que ya ocasionó 160 millones de contagios en todo el mundo y se cobró la vida de más de 3,3 millones de personas, de acuerdo a datos del Johns Hopkins University & Medicine Resource Center, y ante la falta, aún, de disponibilidad de vacunas en muchos países, en el último tiempo en el campo científico se comenzó a analizar la posibilidad de combinar diferentes fármacos, ante la eventual escasez de la segunda dosis de determinada formulación. Pero, ¿es seguro?
Todas las vacunas contra el nuevo coronavirus ampliamente disponibles, con la excepción de la de Johnson & Johnson de una sola inyección, requieren dos dosis. La primera prepara el sistema inmunológico y la segunda (generalmente, administrada unas semanas después) lo refuerza. La perspectiva de combinar dosis de vacunas ofrece la oportunidad de reforzar los lanzamientos de inoculantes y, potencialmente, aumentar la inmunidad proporcionada.
Algunos expertos se preguntan si la flexibilidad para permitir la vacunación de dosis mixtas podría ayudar a las personas a vacunarse por completo más rápido. Otros sostienen que mezclar dos vacunas diferentes podría hacer un mejor trabajo de protección contra el COVID-19. Muchos, en tanto, se mantienen escépticos. Sin embargo, el tema está en análisis.
Según los hallazgos preliminares de un estudio difundido esta semana en la revista especializada The Lancet, alternar dosis de diferentes vacunas contra el coronavirus provoca reacciones leves y moderadas más frecuentes que si se siguen los calendarios estándares de vacunación, con dos inyecciones del mismo preparado.
Un equipo liderado por especialistas de la Universidad Oxford, en Inglaterra, inició una investigación a principio de año con el objetivo de indagar sobre los efectos de la combinación de dos dosis de preparados fabricados por distintas farmacéuticas y encontró que aumentaba los efectos secundarios comunes esperables de una vacuna, como escalofríos, fiebre, dolor muscular en el lugar de la aplicación y fatiga.
Los expertos hallaron que cuando se dejaba entre las dosis un intervalo de cuatro semanas, aplicar combinaciones (Pfizer-BionNTech, seguido de Oxford-AstraZeneca y Oxford-AstraZeneca, seguido de Pfizer-BioNTech) generaba más reacciones leves o moderadas tras la segunda dosis que si se atendía al procedimiento estándar de no combinar diferentes inoculantes.
“Aunque se trata de una parte secundaria de lo que estamos intentado explorar mediante estos estudios, es importante que informemos a la gente acerca de estos datos, especialmente porque varios países están planteándose emplear estos calendarios de dosis mixtas”, sostuvo Matthew Snape, profesor asociado de Pediatría y Vacunas en la Universidad de Oxford, e investigador Jefe del estudio.
“Los perfiles hematológicos y bioquímicos fueron similares entre los programas de vacunación heteróloga y homóloga, con todos los eventos adversos de laboratorio de gravedad de grado 2 o menos en el programa de vacunación heteróloga y sin trombocitopenia en ningún grupo el día siete después de la dosis de refuerzo”, detalla el estudio publicado en The Lancet.
Los expertos también observan que los datos recabados de sus pruebas fueron extraídos de participantes mayores de 50 años, por lo que sostienen que existe la posibilidad de que estas reacciones puedan resultar más prevalentes en grupos etarios más jóvenes.
Los hallazgos del estudio sugieren que “los calendarios de dosis mixtas podrían resultar en un incremento en las ausencias laborales el día después de la inmunización, y es importante considerarlo a la hora de planear la inmunización de los empleados del cuidado sanitario”, agregó Snape.
Sin embargo estas conclusiones son parciales. Las conclusiones finales del trabajo sobre la eficacia o seguridad estarán listas después de junio. El motivo es que, de los 830 voluntarios reclutados, a casi la mitad les administrarán la segunda dosis a los 84 días de la primera. Los datos publicados The Lancet se basan en los resultados preliminares que provocan las vacunas entre la otra mitad, la que recibió las dos dosis en un lapso de 28 días.
El concepto de combinar las vacunas —a veces llamado estímulo primario heterólogo— no es algo nuevo. Durante décadas, los científicos han investigado esta estrategia con la esperanza de hallar combinaciones eficaces contra toda una serie de virus como el de la influenza, el VIH y el del ébola.
“La intercambiabilidad entre las vacunas es y ha sido a lo largo del tiempo un área de interés en la vacunología porque facilita mucho desde lo operativo; beneficia el cumplimiento de los programas de vacunación y evita oportunidades perdidas. Sin embargo, una característica de estas vacunas es que, por ahora, se aconseja no intercambiarlas. Por eso, si bien se trata de una iniciativa más que interesante, sería importante constatar que puedan ser intercambiables. Desde lo hipotético parece plausible”, había explicado recientemente consultado por este medio Francisco Nacinovich, jefe de Infectología del Instituto Cardiovascular de Buenos Aires y miembro de la comisión de vacunas de la Sociedad Argentina de Infectología.
La OMS confirmó la seguridad de la vacuna de AstraZeneca
Luego de que a principios de este mes algunos países europeos cuestionaran la aplicación de la vacuna elaborada por el laboratorio AstraZeneca y la Universidad de Oxford en adultos mayores y esta semana se conocieran casos de de trombosis y coágulos sanguíneos en personas que habían sido vacunadas con esa formulación, hoy la Organización Mundial de la Salud (OMS) aseguró que no hay razón para no usarla.
Asimismo, la Agencia Europea de Medicamentos (EMA) ayer se pronunció acerca de la decisión de la Autoridad Sanitaria Danesa de detener su campaña de vacunación con la vacuna COVID-19 AstraZeneca por los eventos de trombosis mencionados.
“Actualmente, no hay indicios de que la vacunación haya causado estas afecciones, que no figuran como efectos secundarios de esta vacuna. La posición del comité de seguridad de la EMA es que los beneficios de la vacuna continúan superando sus riesgos y la vacuna puede continuar administrándose mientras se está investigando los casos de eventos tromboembólicos”, informó el organismo en un comunicado. Ya se están revisando todos los casos de eventos troboembólicos y otras afecciones relacionadas con los coágulos de sangre, notificados después de la vacunación con la vacuna COVID-19 AstraZeneca", agregaron.
En tanto desde el laboratorio informaron que un análisis de sus datos de seguridad de más de 10 millones de registros “no ha mostrado evidencia de un mayor riesgo de embolia pulmonar o trombosis venosa profunda en ningún grupo de edad definido, género, lote o en ningún país en particular con la Vacuna COVID-19 AstraZeneca”. “De hecho, el número observado de este tipo de eventos es significativamente menor en los vacunados que lo que cabría esperar entre la población general”, reforzaron en un parte de prensa difundido por la compañía.
“En nuestro país, la vacuna COVID-19 AstraZeneca fue autorizada como producto para uso de emergencia el 30 de diciembre por la Anmat. Se puede administrar en mayores de 60 años, porque se siguió la recomendación de la OMS en base a evidencias que demuestran que la vacuna tiene un perfil seguro”, afirma la doctora Ángela Gentile, miembro de la Comisión Nacional de Seguridad en Vacunas de la Argentina en oportunidad de que se pusiera en duda la seguridad de la formulación en adultos mayores.
Al país arribaron el 17 de febrero 580 mil dosis de la vacuna Covishield, la formulación de AstraZeneca/Oxford fabricada en India (el 9 de ese mismo mes las autoridades sanitarias habían autorizado su uso de emergencia) y según informaron desde la cartera sanitaria, al día de hoy fueron distribuidas 547.500 dosis y aplicadas 468.061, tal como figura en el Registro Federal de Vacunación Nominalizado Nomivac.
La vacuna Covishield se produce en el Serum Institute de la India a partir de un acuerdo de colaboración en el contexto de una transferencia tecnológica del laboratorio anglosueco y la universidad británica. El Estado argentino acordó la adquisición de un total de 1.160.000 dosis. Otras 580 mil llegarían en el transcurso de este mes en una aerolínea privada.
Astrazeneca hizo público los resultados de efectividad de su vacuna
Astrazeneca ha hecho públicos los primeros resultados preliminares de efectividad de su vacuna contra el Covid-19, ChAdOx1, en vida real, concretamente de su primera dosis. Los datos, procedentes de la campaña de vacunación en Escocia, revelan una reducción de las hospitalizaciones derivadas del coronavirus en un 94 por ciento en los 28-34 días posteriores a su administración en un grupo poblacional compuesto “en su mayoría” por adultos mayores de 65 años.
El resultado de este estudio, realizado por el servicio público de salud escocés, ha contado con una muestra superior a 1,1 millones de sujetos (35% de la población) mayor de 18 años. En ellos, además del sustancial ‘freno’ a los casos de Covid-19 más graves, se analiza su efectividad combinada con otras vacunas. En ese supuesto “se obtuvieron resultados similares en todos los grupos de edad, incluidas las personas 80 años o más”.
Astrazeneca ha asegurado que los nuevos datos ofrecidos proporcionan “evidencia adicional que refuerza los resultados obtenidos en el análisis combinado de los ensayos clínicos realizados en Reino Unido, Brasil y Sudáfrica”. En ellos no se han apreciado hospitalizaciones o infecciones graves pasados 22 días de la administración de la vacuna de Astrazeneca.
Esta nueva evidencia, además, reabre el debate sobre las posibles limitaciones en la inoculación de la pauta vacunal. En ese sentido, cabe recordar que en la actualidad la mayor parte de los países europeos no usan la ChAdOx1 en toda la población – en España la limitación está en los 55 años- debido a la falta de datos en personas mayores. Los nuevos datos han provocado que Alemania se plantee un cambio de criterio sobre el que, por el momento, no se han pronunciado ni la autoridad europea encargada, la EMA, ni el Ministerio de Sanidad español a través de la Agencia Española de Medicamentos y Productos Sanitarios (Aemps).
Ana Pérez, directora médica de AstraZeneca España, ha declarado que “este estudio ofrece datos esperanzadores sobre el impacto de la vacunación frente a la pandemia de COVID-19. Son unos primeros datos que sugieren una significativa reducción de hospitalizaciones y enfermedad grave por COVID-19 y que nos sitúa más cerca del objetivo común: evitar que la COVID-19 siga amenazando la vida de las personas en todo el mundo”.
Eficacia de la vacuna de AstraZeneca frente a la Covid-19
La eficacia de la vacuna fue del 59,5% (IC95%: 45,8%-69,7%) en los participantes que recibieron las dos dosis recomendadas con un intervalo entre dosis de 4 a 12 semanas.
Los resultados de los un análisis combinado de los ensayos clínicos en fase II/III en Reino Unido, Brasil y Sudáfrica publicados el pasado 19 de febrero en The Lancet muestran que:
- Tras la primera dosis (>22 días) se muestra una eficacia de la vacuna del 76% (IC: 59% a 86%) manteniendo la protección hasta la segunda dosis.
- La eficacia tras la segunda dosis aumenta hasta un 82% (IC: 63%, 92%) cuando la segunda dosis se administra con un intervalo entre dosis de 12 semanas o más.
- El Grupo Consultivo Estratégico de Expertos (SAGE) de la Organización Mundial de la Salud (OMS), encargado de estudiarla, ha asegurado también que la vacuna resulta eficaz frente a la cepa británica
COVAX comenzará a entregar vacunas de AstraZeneca
La Organización Panamericana de la Salud (OPS) informó que COVAX — coalición liderada por la OMS y Gavi para asegurar el acceso equitativo a las vacunas contra la COVID-19 — notificó a países de las Américas sobre la dotación estimada de dosis para la primera fase de entrega de vacunas contra la COVID-19, a través de una carta a sus autoridades de salud. Recibieron dicha carta 36 países y territorios que participan en COVAX -entre ellas la Argentina- con información sobre el número estimado de dosis de la vacuna de AstraZeneca que podrían recibir a partir de la segunda mitad de febrero y a lo largo del segundo trimestre de 2021.
La vacuna de AstraZeneca aún está bajo el análisis de la OMS para recibir la aprobación de uso de emergencia (EUL, por sus siglas en inglés), lo cual se espera pueda ocurrir en los próximos días. El número de dosis y el calendario de entrega están aún sujetos a la EUL, la capacidad de manufacturar la producción, así como del establecimiento de acuerdos de suministro entre los productores, la OPS y la UNICEF. De acuerdo con el comunicado de COVAX, se estima que estarán llegando a las Américas alrededor de 35.3 millones de dosis en esta primera etapa.
“Con más de 45 millones de casos confirmados y más de un millón de muertes, los países y territorios a lo largo de las Américas, y particularmente los más pobres, están pasando por una crisis de salud, económica y social sin precedentes”, dijo la Dra. Carissa F. Etienne, directora de la OPS.
Los países y territorios de las Américas que participan en el mecanismo COVAX y recibieron cartas son: Antigua y Barbuda, Argentina, Bahamas, Barbados, Belice, Bermuda, Bolivia, Brasil, Canadá, Chile, Colombia, Costa Rica, Dominica, Ecuador, El Salvador, Federación de San Cristóbal y Nieves, Granada, Guatemala, Guyana, Haití, Honduras, Islas Vírgenes Británicas, Jamaica, México, Montserrat, Nicaragua, Panamá, Paraguay, Perú, República Dominicana, San Vicente y las Granadinas, Santa Lucía, Surinam, Trinidad y Tobago, Uruguay y Venezuela.
El Fondo Rotatorio de la OPS, junto con la UNICEF, son los encargados de realizar las adquisiciones de todas las vacunas en representación del mecanismo COVAX.
La región de las Américas requerirá inmunizar a aproximadamente 500 millones de personas para controlar la pandemia. El mecanismo COVAX es un esfuerzo global para acelerar el acceso equitativo a las vacunas contra la COVID-19.
La meta es suministrar vacunas para al menos el 20% de la población de cada país participante en el mecanismo COVAX para proteger a las personas en mayor riesgo de presentar formas graves de COVID-19. En América Latina y el Caribe, 37 países recibirán vacunas a través del mecanismo COVAX, de los cuales 27 lo harán con financiamiento propio y 10 lo harán sin costo debido a su condición económica o el tamaño de su población.
Preocupan las mutaciones y piden acelerar la vacunación
El coronavirus no solo es noticia por el daño que genera sino también por las nuevas variantes que presenta. La de Reino Unido, Río de Janeiro, Sudáfrica, China. Los especialistas explican que existe una preocupación mundial por estas mutaciones aunque aclaran que, hasta el momento, no son estructurales por lo que no afectan la eficacia de las vacunas disponibles. Roberto Debbag, vicepresidente de la Sociedad Latinoamericana de Infectología Pediátrica, plantea la existencia de “dos carreras”, una la está dando el virus para transformarse. La otra tiene que ver con las vacunas “efectivas y seguras” y su capacidad de llegar a mucha gente en poco tiempo.
A mi entender, el virus tiene como meta transformarse en otro virus. Va generando nuevas variantes. En algunas personas con dificultades inmunitarias permanece más tiempo y se va reconvirtiendo, sostiene Debbag. Y asegura que el objetivo del virus es que el mundo vuelva a foja cero. Según Debbag, existen vacunas efectivas y seguras y sería importante acelerar la inmunización para ganarle la carrera al virus.
Hay documentos de la vacuna de Pfizer y la de Moderna que muestran que siguen siendo efectivas en la lucha contra el coronavirus. Sería clave que lleguen pronto a un número importante de personas, señala Debbag. Y dice que, mientras tanto, hay que testear y aislar para así evitar que el virus se siga propagando.
El especialista comparte como ejemplo la situación en Israel: Ya lograron vacunar al 78% de los mayores de 70 años y a los trabajadores de la salud. Y ahora están empezando a dársela a personas más jóvenes. Ya detectaron que a la tercera semana de aplicar la primera dosis de la vacuna de Pfizer se reduce en un 50% la transmisión de la enfermedad en las personas inmunizadas, aporta. La velocidad con la que están apareciendo nuevas variantes es una preocupación mundial. Hay que actuar rápido, insiste.
Menciona a AstraZeneca como otra opción viable para la inmunización. Sobre la Sputnik y las nuevas variantes afirma que no hay información. Es probable que la vacuna rusa sirva, pero la realidad es que no tenemos datos precisos, agrega.
Para el infectólogo Eduardo López, jefe del Departamento de Medicina del Hospital Ricardo Gutiérrez, los coronavirus tienen frecuentes mutaciones, una o dos mensuales, no muy significativas en cuanto a lo genético.
La variante de Reino Unido es, hasta ahora, la más relevante. Esto tiene que ver con que tiene más capacidad de evadir el sistema inmune y mayor transmisibilidad, aunque no del 70% como se creía al principio sino del 35%, según el último informe del sistema de salud oficial de Inglaterra, cuenta López.
Que genere nuevas mutaciones es algo que preocupa, más que nada a partir del caso de Reino Unido. Por ahora no son estructurales, esto quiere decir que las vacunas disponibles siguen siendo útiles. El Instituto Gamaleya declaró que la Sputnik cubre las nuevas variantes, detalla el infectólogo del Hospital Ricardo Gutiérrez.
Y explica que incluso varios desarrolladores confirmaron que estarían en condiciones de adaptar sus vacunas en caso de que apareciera una nueva cepa. Lo dijeron desde Pfizer, AstraZeneca y Gamaleya, sostiene. Explica que esto puede hacerse a partir de la “secuenciación del virus”. Es posible ver qué es lo que se modificó y, en base a eso, diseñar una nueva vacuna, suma.
Hasta lograr la inmunidad de rebaño, para frenar la curva de contagios hay que apelar a un comportamiento social preventivo, que incluye distanciamiento, barbijo y alcohol en gel, sigue López. Además, debemos incrementar los testeos, aislar casos positivos, buscar contactos estrechos y vacunar, especialmente a los mayores de 60 años, precisa.
Segundo año consecutivo de la campaña "Más que Glucosa"
Por segundo año consecutivo, se lanza en el país la campaña “Más que glucosa”. Bajo la premisa “Hay órganos que sufren y no se ven”, se busca concientizar a la población argentina sobre la importancia de un tratamiento integral de la diabetes. Este no se trata sólo de controlar los niveles de glucosa en sangre, ya que existe una alta prevalencia de complicaciones cardiovasculares y renales que son independientes del control glucémico.
El corazón y el riñón son dos órganos fundamentales y su daño empeora el pronóstico de las personas con diabetes y afecta profundamente su calidad de vida. El 40% de las personas con esta patología puede deteriorar su función renal en algún momento de su vida, siendo la diabetes la primera causa de diálisis en nuestro país. Por otro lado, hasta un 68% de las personas con diabetes pueden presentar algún grado de disfunción cardíaca. Una vez que se desarrolla insuficiencia cardíaca con síntomas, la mortalidad es del 50% a 5 años, similar a algunos tipos de cáncer.
Esta campaña de concientización está desarrollada en conjunto por la Sociedad Argentina de Diabetes, la Sociedad Argentina de Cardiología, Federación Argentina de Cardiología, la Sociedad Argentina de Medicina, la Sociedad Argentina de Nefrología y el laboratorio AstraZeneca, con el fin de brindar información de interés para los pacientes, familiares, comunidad médica y la sociedad en general poniendo el foco que en la diabetes hay órganos que sufren y que no se ven.
La campaña cuenta con una plataforma de información www.masqueglucosa.com.ar la cual brindará de manera continua material de fácil comprensión para que cualquier persona conozca más a fondo las causas, recomendaciones médicas, datos de alimentación y ejercicio físico, consejos para bajar el índice glucémico, e información sobre las posibles enfermedades y complicaciones asociadas a la diabetes. También se puede obtener información a través de las redes sociales en Instagram y Facebook (@masqueglucosa /masqueglucosa).
“Saber que la diabetes tipo 2 es una enfermedad silenciosa y puede no presentar síntomas nos ayuda a intervenir mucho antes, buscando diagnosticarla precozmente e intervenir para evitar su progresión y sus complicaciones. En nuestro país fallecen más de 8000 personas por año por diabetes y es una de las enfermedades previas que conllevan mayor riesgo de severidad en la actual pandemia de coronavirus”, declaró la Dra. Graciela Fuente, Presidente de la Sociedad Argentina de Diabetes.
“El objetivo de esta campaña es acompañar e informar a las personas con diabetes y sus familias. Además de llevar un control continuo por parte de un profesional, es muy importante tener acceso a información de guía. Esperamos poder ser un aporte para sobrellevar de mejor manera la diabetes, especialmente en este contexto donde más que nunca se necesita información veraz, generada por expertos en la materia y de libre acceso”, expresó el Dr. José Luis Navarro Estrada, presidente de la Sociedad Argentina de Cardiología.
La diabetes se relaciona con el rápido aumento del sobrepeso y la obesidad, favorecidos por la alimentación inadecuada, el sedentarismo y la actividad física insuficiente. En todo el mundo, 463 millones de personas la tienen y se estima que ese número se elevará a 700 millones en el año 2045. Se estima que la diabetes afecta a más de 3.000.000 de personas en nuestro país y dado que por varios años permanece silenciosa, aproximadamente la mitad de quienes la tienen, desconocen su condición. Según la 4ta Encuesta Nacional de Factores (ENFR) de riesgo 2019, el 12,7% de la población tiene diabetes o glucemia elevada, registrando un aumento significativo con respecto a la 3° ENFR (9,8%).
Un control periódico con el médico es fundamental para evitar la aparición y la progresión de las enfermedades asociadas a la diabetes. Además, es importante mantener un estilo de vida saludable, evitar el sedentarismo, seguir una buena alimentación y evitar el consumo excesivo de sal. Para mejorar el pronóstico de los pacientes, es esencial cuidar los factores de riesgo, un diagnóstico temprano y adecuados tratamientos que ayuden a prevenir la aparición de los efectos de la diabetes en el riñón y en el corazón.
En este contexto de pandemia por el coronavirus, las personas con diabetes forman parte del grupo de riesgo ya que, luego de la hipertensión, los pacientes con esta enfermedad tienen mayor probabilidad de presentar complicaciones severas al contagiarse de Covid-19. Por ello, es importante no abandonar los tratamientos indicados por el médico, continuarlos de forma habitual y consultarle ante cualquier duda.
AstraZeneca: suspende ensayo de vacuna y sufre bajas en la bolsa
El laboratorio AstraZeneca frenó las pruebas de la vacuna contra el coronavirus que desarrolla con la Universidad de Oxford, y que será producida en Argentina, debido a "posibles reacciones adversas" en uno de los participantes del estudio durante la fase 3 de los testeos.
El laboratorio sueco-británico hizo un alto en sus pruebas y revisará los resultados a fin de poder avanzar en el desarrollo de la vacuna, la cual será producida por Argentina y México en Latinoamérica.
Un portavoz de la compañía afirmó que "el proceso de revisión provocó una pausa en la vacunación para permitir la revisión de los datos de seguridad".
Previamente, en las etapas 1 y 2 de las pruebas, en julio, el laboratorio había comunicado que el 60% de los mil voluntarios que recibieron la vacuna experimentaron efectos secundarios como fiebre y dolor de cabeza y muscular, entre otros.
Sin embargo, aquellos malestares solo fueron considerados como consecuencias lógicas de los cambios generados por la vacuna en el organismo de los participantes del estudio, y fueron menguando conforme avanzó el tiempo.
En agosto pasado, el presidente Alberto Fernández había anunciado que Argentina sería uno de los países de la región que habían sido seleccionados para producir la vacuna de AstraZeneca y Oxford, una de las tantas que buscan ser efectivas contra el Covid-19 en todo el mundo.
Asimismo Las acciones del laboratorio AstraZeneca caen 6,6% en el after market de Wall Street después de conocerse que la firma debió suspender sus ensayos de la vacuna contra el Covid-19, al encontrar una reacción adversa en un participante del estudio.
Argentina y México generarán la vacuna de Oxford contra el covid-19 para Latinoamérica
Argentina y México producirán la vacuna contra el nuevo coronavirus desarrollada por la Universidad de Oxford y la empresa farmacéutica AstraZeneca que se distribuirá para Latinoamérica, anunció hoy el Presidente de la Nación, Alberto Fernández, lo que permitirá que el país pueda tener prioridad a la hora de acceder a la misma. Se estima que la potencial vacuna de AstraZeneca-Oxford estará disponible para el primer semestre de 2021.
El Presidente explicó que AstraZeneca eligió al laboratorio argentino mAbxience para producir el principio activo de la vacuna, lo que “es un inmenso desafío para la industria nacional y México será el encargado de envasar la vacuna y finalmente se distribuirá de forma equitativa según la demanda de cada país”.
El mandatario destacó que el acuerdo entre el laboratorio AstraZeneca con el apoyo de la Fundación Slim “es un proyecto sin fines de lucro que nos han permitido acceder a una vacuna a un precio razonable de 3 a 4 dólares por dosis”, al tiempo que subrayó que “es un gran alivio para el futuro, pero no es una solución para el presente”.
“Es una gran noticia que México y Argentina sean los puntos referenciales en la producción de esta vacuna y que sea una solución para el continente. Seguimos trabajando con otros proveedores para ver primero cuál es la más efectiva, y segundo cuándo podemos contar con ella”, sostuvo Fernández al referirse a las otras opciones de vacunas que se encuentran en estudio.
El ministro de Salud de la Nación, Ginés González García, se mostró “contento porque estamos tratando de asegurar el acceso a la vacuna y una manera de asegurarlo es que el precio sea razonable. Estamos orgullosos porque no es fácil producir la materia prima de una vacuna de esta complejidad”.
El titular de la cartera sanitaria nacional, quien estuvo acompañado por la secretaria de Acceso a la Salud, Carla Vizzotti, señaló que “tener la capacidad de producción local, no solo es una muy buena noticia para toda Latinoamérica, sino que también es una seguridad de acceso a la vacuna en tiempo y forma”.
Las autoridades además adelantaron que habrá prioridades para el acceso a la vacuna, entre los que se encuentran los trabajadores de salud y las personas con patologías previas.
Durante la reunión con AstraZeneca, previa al anuncio, Agustín Lamas, Presidente de la firma para la Región del Cono Sur comentó: “este acuerdo destaca el gran nivel de profesionales, la calidad de la ciencia y las capacidades de fabricación que tiene nuestro país. Si los ensayos clínicos resultasen resultados positivos, esta alianza estratégica proporcionará acceso temprano a la potencial vacuna COVID-19 para Argentina”.
Desde el laboratorio estiman llegar a un piso de producción de 150 millones de dosis y un techo de 250 millones. Se calcula que en Latinoamérica, excluyendo a Brasil, se van a necesitar 230 millones de dosis.
El pasado 20 de julio se publicó en la revista científica The Lancet un estudio hecho con 1077 voluntarios -adultos sanos de entre 18 y 55 años- que mostró que la vacuna de Oxford es segura y una dosis generó en el 95 por ciento de los participantes un aumento en los anticuerpos contra el virus SARS-CoV-2, causante de la COVID-19.
Actualmente la vacuna se encuentra desarrollando los estudios de Fase III lo que la posiciona como la vacuna más adelantada.
Lo más visto
- Covishield, la vacuna que India lanzó con Oxford-AstraZeneca
- El gobierno establece los requisitos para la producción de cannabis medicinal
- Anmat aprobó en el país la primera vacuna que protege contra el dengue
- Comunicación de Novo Nordisk: Diferencias en la indicación de Victoza® y Saxenda®
- Ibupirac declarado apto para celíacos